Wir erforschen den Boden/Wir ermitteln den Kalkgehalt eines Bodens durch Kohlenstoffdioxid-Volumenmessung: Unterschied zwischen den Versionen
Aus ZUM-Unterrichten
Main>Cereale Keine Bearbeitungszusammenfassung |
Main>Cereale Keine Bearbeitungszusammenfassung |
||
| Zeile 1: | Zeile 1: | ||
{{Boden}} | |||
{{Boden | '''Informationen zum Thema und Untersuchungsmaterialien''' | ||
Wenn Salzsäure auf Calziumcarbonat trifft, wird Kohlenstoffdioxid freigesetzt.Das Kohlenstoffdioxid-Volumen lässt sich im Kolbenprober bestimmen. | |||
'''Untersuchungsmaterialien''' | '''Untersuchungsmaterialien''' | ||
| Zeile 32: | Zeile 12: | ||
* Bodenproben | * Bodenproben | ||
<center> | <center> | ||
| Zeile 41: | Zeile 20: | ||
'''Versuchsablauf''' | |||
* a) Baue die Apparatur auf. | |||
* b) Fülle 20 g Boden in den Erlenmeyerkolben. | |||
* c) Fülle 20 ml Salzsäure in den Scheidetrichter. Öffne den Hahn; die Salzsäure fließt auf die Bodenprobe. Den Hahn sofort wieder schließen. Wenn keine Blasen mehr aufsteigen, ist die Gasbildung beendet. | |||
* d) Stelle die gewonnene Kohlenstoffdioxid-Menge fest. | |||
* e) Werte aus! | |||
'''Erfahrungen und Konsequenzen''' | |||
Der Versuch ist als Schüler-Partnerversuch geeignet. Das Verfahren ist durch erhebliche methodische Fehlerquellen beeinträchtigt: | |||
* Das Kohlenstoffdioxid sollte auf möglichst '''kurzem Wege''' in den Kolbenprober gelangen. | |||
* Beim Umgang mit Erde werden die Dichtungsstellen verunreinigt und neigen zur Undichtigkeit (Trichter verwenden!). | |||
* Vor dem Ablesen den Stempel hin- und herdrehen, sonst besteht die Gefahr, dass der Reibungswiderstand die Messwerte verfälscht. | |||
* Zu Demonstrationszwecken sollte eine carbonatreiche Bodenprobe entgast werden. | |||
'''Verständnisfragen zum Experiment "Wir ermitteln den Kalkgehalt eines Bodens durch Kohlenstoffdioxid-Volumenmessung ''' | |||
* 1. Was hast du in diesem Experiment getan? | |||
* 2. Wie kann man von der Kohlenstoffdioxid-Menge auf den Kalkgehalt eines Bodens schließen? | |||
* 3. Wo können Fehlerquellen bei diesem Experiment auftreten? | |||
| | ||
<Center> | <Center> | ||
Version vom 20. Mai 2009, 07:08 Uhr
Wir erforschen den Boden
Einfache Analyseverfahren
Organische Zusammensetzung
- Humusanteil
- Bakterienkunde
- Lichtmikroskop
- Plattengussverfahren
- Bakterienkeimzahl
- Bodenpilze
- Kohlenstoffdioxidbildung
- Regenwurm
Bodenwasser, -luft, -wärme
Bodenreaktion
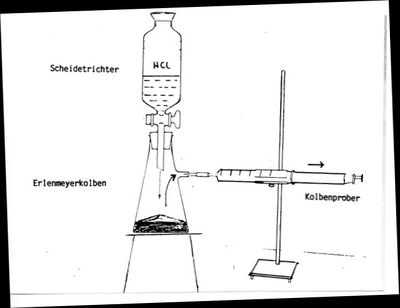
Informationen zum Thema und Untersuchungsmaterialien Wenn Salzsäure auf Calziumcarbonat trifft, wird Kohlenstoffdioxid freigesetzt.Das Kohlenstoffdioxid-Volumen lässt sich im Kolbenprober bestimmen.
Untersuchungsmaterialien
- Scheidetrichter
- Kolbenprober
- Erlenmeyerkolben mit seitlichem Ansatz (250 ml)
- Bodenproben
Versuchsablauf
- a) Baue die Apparatur auf.
- b) Fülle 20 g Boden in den Erlenmeyerkolben.
- c) Fülle 20 ml Salzsäure in den Scheidetrichter. Öffne den Hahn; die Salzsäure fließt auf die Bodenprobe. Den Hahn sofort wieder schließen. Wenn keine Blasen mehr aufsteigen, ist die Gasbildung beendet.
- d) Stelle die gewonnene Kohlenstoffdioxid-Menge fest.
- e) Werte aus!
Erfahrungen und Konsequenzen
Der Versuch ist als Schüler-Partnerversuch geeignet. Das Verfahren ist durch erhebliche methodische Fehlerquellen beeinträchtigt:
- Das Kohlenstoffdioxid sollte auf möglichst kurzem Wege in den Kolbenprober gelangen.
- Beim Umgang mit Erde werden die Dichtungsstellen verunreinigt und neigen zur Undichtigkeit (Trichter verwenden!).
- Vor dem Ablesen den Stempel hin- und herdrehen, sonst besteht die Gefahr, dass der Reibungswiderstand die Messwerte verfälscht.
- Zu Demonstrationszwecken sollte eine carbonatreiche Bodenprobe entgast werden.
Verständnisfragen zum Experiment "Wir ermitteln den Kalkgehalt eines Bodens durch Kohlenstoffdioxid-Volumenmessung
- 1. Was hast du in diesem Experiment getan?
- 2. Wie kann man von der Kohlenstoffdioxid-Menge auf den Kalkgehalt eines Bodens schließen?
- 3. Wo können Fehlerquellen bei diesem Experiment auftreten?
Umrechnungstabelle Kohlenstoffdioxid-Milliliter in Kohlenstoffdioxid -Milligramm |