Chemie-Lexikon/Dichte: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
(- {{Video) Markierung: Quelltext-Bearbeitung 2017 |
||
| (5 dazwischenliegende Versionen von 2 Benutzern werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
{{SORTIERUNG:{{SUBPAGENAME}}}} | |||
==Worum geht es hier== | ==Worum geht es hier== | ||
Wenn etwas im Wasser untergeht sagt man gerne ''"das war zu schwer"''. Aber, was ist mit ganzen Baumstämmen? Sind die leicht, weil sie nicht untergehen? Nein, das kann es nicht sein, denn sicher ist ein großer Baumstamm nicht gerade leicht. Und dann geht ja selbst der leichteste Stein im Wasser unter. | Wenn etwas im Wasser untergeht sagt man gerne ''"das war zu schwer"''. Aber, was ist mit ganzen Baumstämmen? Sind die leicht, weil sie nicht untergehen? Nein, das kann es nicht sein, denn sicher ist ein großer Baumstamm nicht gerade leicht. Und dann geht ja selbst der leichteste Stein im Wasser unter. | ||
<gallery heights="220px" mode="packed" style="text-align:center" > | <gallery heights="220px" mode="packed" style="text-align:center"> | ||
Datei:Floss.jpg|Große Holzstücke schwimmen ... | |||
Datei:Aberdesach MMB 06.jpg|... aber selbst die kleinesten Steinchen gehen unter. | |||
</gallery> | </gallery> | ||
| Zeile 20: | Zeile 21: | ||
{| class="wikitable" | {| class="wikitable" | ||
|- | |- | ||
! Stoff !! Masse von 1 cm³ | !Stoff!!Masse von 1 cm³ | ||
|- | |- | ||
| Eisen || 7,874 g/cm³ | |Eisen||7,874 g/cm³ | ||
|- | |- | ||
| Aluminium || 2,6989 g/cm³ | |Aluminium||2,6989 g/cm³ | ||
|- | |- | ||
| Blei || 11,342 g/cm³ | |Blei||11,342 g/cm³ | ||
|- | |- | ||
| Holz <br> <small>''(je nach Holzart)''</small>|| z.B. zwischen 0,47 g/cm³ (Fichte) und 0,69 g/cm³ (Esche) | |Holz <br> <small>''(je nach Holzart)''</small>||z.B. zwischen 0,47 g/cm³ (Fichte) und 0,69 g/cm³ (Esche) | ||
|- | |- | ||
| Kunststoff <br> ''(z.B.Poylethylen)'' || zwischen 0,915 g/cm³ und 0,97 g/cm³ | |Kunststoff <br> ''(z.B.Poylethylen)''||zwischen 0,915 g/cm³ und 0,97 g/cm³ | ||
|- | |- | ||
| usw. || ... | |usw.||... | ||
|} | |} | ||
</div> | </div> | ||
| Zeile 54: | Zeile 55: | ||
Die '''DICHTE''' ''(oder auch spezifisches Gewicht)'' ist eine Stoffeigenschaft, die für viele reine Stoffe genau bestimmt werden kann. Daher kann man die Dichte auch nutzen, um einen Stoff zu identifizieren. Damit man nicht immer selber die Dichte berechnen muss, gibt es die Werte von ganz vielen Stoffen in Datensammlungen, in denen du nachschlagen kannst. | Die '''DICHTE''' ''(oder auch spezifisches Gewicht)'' ist eine Stoffeigenschaft, die für viele reine Stoffe genau bestimmt werden kann. Daher kann man die Dichte auch nutzen, um einen Stoff zu identifizieren. Damit man nicht immer selber die Dichte berechnen muss, gibt es die Werte von ganz vielen Stoffen in Datensammlungen, in denen du nachschlagen kannst. | ||
In der Wikipedia findest du zu fast jedem Stoff, der dort aufgeführt ist, immer auch die Dichte, da es eine wichtige Stoffeigenschaft ist. Schul-Bücher enthalten meist eine Liste der Elemente mit Eigenschaften, in denen meist auch die Dichten angegeben sind. Einen Überblick liefern die Tabellen hier: | In der Wikipedia findest du zu fast jedem Stoff, der dort aufgeführt ist, immer auch die Dichte, da es eine wichtige Stoffeigenschaft ist. Schul-Bücher enthalten meist eine Liste der Elemente mit Eigenschaften, in denen meist auch die Dichten angegeben sind. Einen Überblick liefern die Tabellen hier: | ||
* [http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_fester_Stoffe Dichte fester Stoffe] - [http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_fl%C3%BCssiger_Stoffe Dichte flüssiger Stoffe] - [http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_gasf%C3%B6rmiger_Stoffe Dichte gasförmiger Stoffe] | |||
*[http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_fester_Stoffe Dichte fester Stoffe] - [http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_fl%C3%BCssiger_Stoffe Dichte flüssiger Stoffe] - [http://de.wikibooks.org/wiki/Tabellensammlung_Chemie/_Dichte_gasf%C3%B6rmiger_Stoffe Dichte gasförmiger Stoffe] | |||
Die Dichte eines Stoffes kann schon helfen, einen Stoff zu identifizieren, daher sollte man auch wissen, wie man die Dichte bei verschiedenen Stoffen bestimmen kann. | Die Dichte eines Stoffes kann schon helfen, einen Stoff zu identifizieren, daher sollte man auch wissen, wie man die Dichte bei verschiedenen Stoffen bestimmen kann. | ||
== Praktische Bestimmung von Dichten == | ==Praktische Bestimmung von Dichten== | ||
Für die Bestimmung der Dichte eines unbekannten Stoffes muss man eine Portion des reinen Stoffes haben und von dieser Portion das Volumen und sein Gewicht bestimmen. Je nachdem, in welchem Aggregatzustand der Stoff vorliegt, führt das zu unterschiedlichen Problemen bei der Bestimmung der beiden Werte. | Für die Bestimmung der Dichte eines unbekannten Stoffes muss man eine Portion des reinen Stoffes haben und von dieser Portion das Volumen und sein Gewicht bestimmen. Je nachdem, in welchem Aggregatzustand der Stoff vorliegt, führt das zu unterschiedlichen Problemen bei der Bestimmung der beiden Werte. | ||
| Zeile 70: | Zeile 72: | ||
Diese Überlegungen zeigen die "Probleme", die es nötig machen, für jeden Aggregatzustand ein spezielles Verfahren zu nutzen, mit denen man das Volumen und die Masse von einer Stoffportion bestimmen kann, um dann die Dichte zu berechnen. | Diese Überlegungen zeigen die "Probleme", die es nötig machen, für jeden Aggregatzustand ein spezielles Verfahren zu nutzen, mit denen man das Volumen und die Masse von einer Stoffportion bestimmen kann, um dann die Dichte zu berechnen. | ||
* [[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Feststoffen|Experiment und Aufgaben zur Dichtebestimmung bei Feststoffen]] | *[[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Feststoffen|Experiment und Aufgaben zur Dichtebestimmung bei Feststoffen]] | ||
* [[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Flüssigkeiten|Experiment und Aufgaben zur Dichtebestimmung bei Flüssigkeiten]] | *[[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Flüssigkeiten|Experiment und Aufgaben zur Dichtebestimmung bei Flüssigkeiten]] | ||
* [[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Gasen|Experiment und Aufgaben zur Dichtebestimmung bei Gasen]] | *[[Chemie/Sammlung_von_Experimenten/Dichtebestimmung_bei_Gasen|Experiment und Aufgaben zur Dichtebestimmung bei Gasen]] | ||
== Aufgaben und Berechnungen mit der Dichte == | ==Aufgaben und Berechnungen mit der Dichte== | ||
Die Dichte ist nicht nur ein Wert, denn man bestimmt, um einen Stoff zu identifizieren. Auch bei bekannter Dichte, gibt es da zahlreiche Anwendungen, wo mit Hilfe der Dichte etwas berechnet werden kann. Hier ein paar schnelle Beispiele: | Die Dichte ist nicht nur ein Wert, denn man bestimmt, um einen Stoff zu identifizieren. Auch bei bekannter Dichte, gibt es da zahlreiche Anwendungen, wo mit Hilfe der Dichte etwas berechnet werden kann. Hier ein paar schnelle Beispiele: | ||
* Welches Volumen hat eine angegebene Masse z.B. von Öl? Das wäre interessant wenn man keine Waage hat, aber ein genaues Messgefäß für das Volumen. | |||
* Umgekehrt kann man bei bekannter Dichte, von der Masse einer Stoffportion auf das Volumen schließen. | *Welches Volumen hat eine angegebene Masse z.B. von Öl? Das wäre interessant wenn man keine Waage hat, aber ein genaues Messgefäß für das Volumen. | ||
* Auch die Berechung der Dichte wäre interessant, wenn man zum Beispiel untersuchen will, ob der Gold-Ring wirklich komplett aus Gold ist oder nur vergoldet. | *Umgekehrt kann man bei bekannter Dichte, von der Masse einer Stoffportion auf das Volumen schließen. | ||
*Auch die Berechung der Dichte wäre interessant, wenn man zum Beispiel untersuchen will, ob der Gold-Ring wirklich komplett aus Gold ist oder nur vergoldet. | |||
Auf der folgenden Unterseite geht es um solche Aufgaben und du erhältst alle Informationen, wie man die Formel für die Defintion der Dichte nutzen kann, um alles zu berechnen. | Auf der folgenden Unterseite geht es um solche Aufgaben und du erhältst alle Informationen, wie man die Formel für die Defintion der Dichte nutzen kann, um alles zu berechnen. | ||
| Zeile 84: | Zeile 87: | ||
'''→ [[Chemie-Lexikon/Stöchiometrie - Berechnungen mit der Dichte|Stöchiometrie - Berechnungen mit der Dichte]]''' | '''→ [[Chemie-Lexikon/Stöchiometrie - Berechnungen mit der Dichte|Stöchiometrie - Berechnungen mit der Dichte]]''' | ||
== Bedeutung der Dichte für den Auftrieb == | ==Bedeutung der Dichte für den Auftrieb== | ||
<div class="grid"> | <div class="grid"> | ||
<div class="width-3-4"> | <div class="width-3-4"> | ||
Das Bild rechts zeigt verschiedene <u>flüssige</u> und <u>feste</u> Stoffe übereinander. Von oben nach unten sind es: | Das Bild rechts zeigt verschiedene <u>flüssige</u> und <u>feste</u> Stoffe übereinander. Von oben nach unten sind es: | ||
* Benzin, rot angefärbter Reinigungsalkohol (''Isopropanol''), Speise-Öl, Wachs, blau gefärbtes Wasser, Aluminium | *Benzin, rot angefärbter Reinigungsalkohol (''Isopropanol''), Speise-Öl, Wachs, blau gefärbtes Wasser, Aluminium | ||
''Was hat das mit der Dichte zu tun?'' | ''Was hat das mit der Dichte zu tun?'' | ||
| Zeile 97: | Zeile 100: | ||
{| class="wikitable" | {| class="wikitable" | ||
|- | |- | ||
! Stoff !! Dichte | !Stoff!!Dichte | ||
|- | |- | ||
| Benzin || 0,748 g/cm³ | |Benzin||0,748 g/cm³ | ||
|- | |- | ||
| Isopropanol || 0,78 g/cm³ | |Isopropanol||0,78 g/cm³ | ||
|- | |- | ||
| Speise-Öl || 0,91 g/cm³ | |Speise-Öl||0,91 g/cm³ | ||
|- | |- | ||
| Wachs || 0,95 g/cm³ | |Wachs||0,95 g/cm³ | ||
|- | |- | ||
| Wasser || 1 g/cm³ | |Wasser||1 g/cm³ | ||
|- | |- | ||
| Aluminium || 2,6989 g/cm³ | |Aluminium||2,6989 g/cm³ | ||
|} | |} | ||
| Zeile 132: | Zeile 135: | ||
<div class="grid"> | <div class="grid"> | ||
<div class="width-2-3">Und da sind wir eigentlich wieder bei unserer ursprünglichen Frage, nämlich '''warum Holz auf Wasser schwimmt'''. Denn die meisten Holzarten (''siehe {{wpde|Holz#Dichte_und_elastomechanische_Eigenschaften|Holz}}'')&nbrsp;haben eine Dichte, die geringer als die vom Wasser ist. Und genau deshalb schwimmt Holz im Wasser. | <div class="width-2-3">Und da sind wir eigentlich wieder bei unserer ursprünglichen Frage, nämlich '''warum Holz auf Wasser schwimmt'''. Denn die meisten Holzarten (''siehe {{wpde|Holz#Dichte_und_elastomechanische_Eigenschaften|Holz}}'')&nbrsp;haben eine Dichte, die geringer als die vom Wasser ist. Und genau deshalb schwimmt Holz im Wasser. | ||
| Zeile 142: | Zeile 145: | ||
<div class="grid"> | <div class="grid"> | ||
<div class="width-2-3">Oder warst du schon mal '''im Meer schwimmen'''? Im Vergleich zu Süßwasser hat das Meerwasser, in dem Salz gelöst ist, eine höhere Dichte und so fällt das Schwimmen im Meer besonders leicht. | <div class="width-2-3">Oder warst du schon mal '''im Meer schwimmen'''? Im Vergleich zu Süßwasser hat das Meerwasser, in dem Salz gelöst ist, eine höhere Dichte und so fällt das Schwimmen im Meer besonders leicht. | ||
| Zeile 153: | Zeile 157: | ||
Dies gilt übrigens nicht nur in Flüssgikeit sondern auch in der Luft. Habe Stoffe ungefähr die gleiche Form, so lassen sich Stoffe mit geringer Dichte leichter wegpusten und fallen weniger langsam runter. | Dies gilt übrigens nicht nur in Flüssgikeit sondern auch in der Luft. Habe Stoffe ungefähr die gleiche Form, so lassen sich Stoffe mit geringer Dichte leichter wegpusten und fallen weniger langsam runter. | ||
| Zeile 159: | Zeile 164: | ||
</div> | </div> | ||
== Wissenwertes rund um die Dichte == | ==Wissenwertes rund um die Dichte== | ||
Nach den schon vorher angesprochenen Beispielen, wie sich die Dichte auswirkt, noch ein paar weitere alltägliche Effekte, wo wir die Dichte zu spüren bekommen. | Nach den schon vorher angesprochenen Beispielen, wie sich die Dichte auswirkt, noch ein paar weitere alltägliche Effekte, wo wir die Dichte zu spüren bekommen. | ||
=== Leicht- und Schwermetall === | ===Leicht- und Schwermetall=== | ||
Den Begriff '''Schwermetalle''' wirst du vielleicht schon mal gehört haben. Meist wird er im Zusammenhang mit Umweltverschmutzung genannt. Schwermetall-Verbindungen sind meist für den Menschen und Tiere ungesund. Man kann sie allerdings nicht so einfach sehen, die Schwermetall-Verbindungen sind Salzartige Stoffe, die im Wasser löslich sind. | Den Begriff '''Schwermetalle''' wirst du vielleicht schon mal gehört haben. Meist wird er im Zusammenhang mit Umweltverschmutzung genannt. Schwermetall-Verbindungen sind meist für den Menschen und Tiere ungesund. Man kann sie allerdings nicht so einfach sehen, die Schwermetall-Verbindungen sind Salzartige Stoffe, die im Wasser löslich sind. | ||
| Zeile 177: | Zeile 182: | ||
Dagegen nutzt man die Leichtmetalle wie {{wpde|Magnesium|Magnesium}} und {{wpde|Aluminium|Aluminium}} zum Beispiel beim Fahrzeugbau um Gewicht und damit Treibstoff zu sparen. | Dagegen nutzt man die Leichtmetalle wie {{wpde|Magnesium|Magnesium}} und {{wpde|Aluminium|Aluminium}} zum Beispiel beim Fahrzeugbau um Gewicht und damit Treibstoff zu sparen. | ||
=== Die Dichteanomalie des Wassers === | ===Die Dichteanomalie des Wassers=== | ||
''Die Dichte von Wasser ist unnormal!?'' Das erscheint dir sicher irgendwie merkwürdig, denn Wasser ist ein so alltäglicher Stoff ... wäre einem da etwas Unnormales nicht schon aufgefallen? | ''Die Dichte von Wasser ist unnormal!?'' Das erscheint dir sicher irgendwie merkwürdig, denn Wasser ist ein so alltäglicher Stoff ... wäre einem da etwas Unnormales nicht schon aufgefallen? | ||
| Zeile 185: | Zeile 190: | ||
Folgendes ist zu erkennen: | Folgendes ist zu erkennen: | ||
* Feste Wachsklumpen gehen in flüssigem Wachs unter → ''die Dichte von festem | |||
* Gefrorener Eiseissig (''= hochkonzentrieter Essig'') geht im flüssigen Eisessig ebenfalls unter → ''die Dichte von festem Eisessig ist geringer als die Dichte von flüssigem Eissessig'' | *Feste Wachsklumpen gehen in flüssigem Wachs unter → '''die Dichte von festem Wachs ist geringer als die Dichte von flüssigem Wachs''' | ||
* Gefrorenes Wasser, also Eis, schwimmt im flüssigen Wasser → ''die Dichte von festem | *Gefrorener Eiseissig (''= hochkonzentrieter Essig'') geht im flüssigen Eisessig ebenfalls unter → '''die Dichte von festem Eisessig ist geringer als die Dichte von flüssigem Eissessig''' | ||
*Gefrorenes Wasser, also Eis, schwimmt im flüssigen Wasser → '''die Dichte von festem Wasser (= Eis) ist höher als die Dichte von flüssigem Wasser''' | |||
Wachs und Eisessig sind hier die eigentlich '''normalen''' Stoffe. Denn bei allen anderen Stoffen, eben außer dem Wasser, ist es so, dass der feste Stoff in seinen flüssigen Aggregatzustand untergeht. Und das ist das Unnormale am Wasser. | Wachs und Eisessig sind hier die eigentlich '''normalen''' Stoffe. Denn bei allen anderen Stoffen, eben außer dem Wasser, ist es so, dass der feste Stoff in seinen flüssigen Aggregatzustand untergeht. Und das ist das Unnormale am Wasser. | ||
| Zeile 207: | Zeile 213: | ||
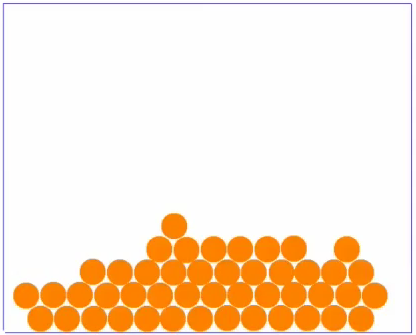
Bei sehr niedrigen Temperaturen ist der '''Stoff fest''' und die Bewegung der Teilchen ist sehr langsam. Die Teilchen sind ganz nah beieinander und eng gepackt. | Bei sehr niedrigen Temperaturen ist der '''Stoff fest''' und die Bewegung der Teilchen ist sehr langsam. Die Teilchen sind ganz nah beieinander und eng gepackt. | ||
Einen Film, bei dem man die Teilchen in Bewegung sieht, findest du [http://www.youtube.com/watch?v=aqSoC_CrmvI hier]. | |||
</div> | </div> | ||
<div class="width-1-3"> | <div class="width-1-3"> | ||
[[Datei:FilmBild-Teilchenmodell flüssig.png]] | [[Datei:FilmBild-Teilchenmodell flüssig.png]] | ||
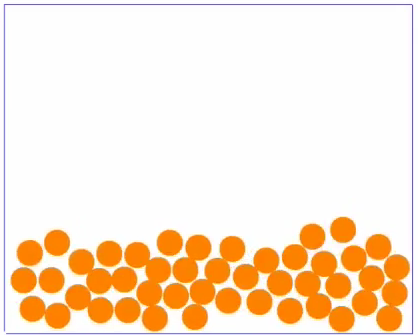
Bei mittleren Temperaturen ist der '''Stoff flüssig''' | Bei mittleren Temperaturen ist der '''Stoff flüssig''' und die Teilchen sind zwar auch noch nah beieinander, da sich aber die Teilchen mit dem Erhitzen des Stoffes schneller bewegen, können sie nicht mehr so eng zusammen bleiben, wie vorher beim festen Stoff. Der von den Teilchen eingenommene Platz ist daher größer. | ||
<small>Ein Film, bei dem man Teilchen in Bewegung sieht findest du | <small>Ein Film, bei dem man die Teilchen in Bewegung sieht, findest du [http://www.youtube.com/watch?v=b4cPktEtw8g hier].</small> | ||
</div> | </div> | ||
<div class="width-1-3"> | <div class="width-1-3"> | ||
| Zeile 221: | Zeile 227: | ||
Bei sehr hohen Temperaturen ist der '''Stoff gasförmig''' und die Teilchen sind noch schneller und daher wird ihr Abstand noch größer und die Teilchen sind weit im Raum verteilt. | Bei sehr hohen Temperaturen ist der '''Stoff gasförmig''' und die Teilchen sind noch schneller und daher wird ihr Abstand noch größer und die Teilchen sind weit im Raum verteilt. | ||
<small>Ein Film, bei dem man Teilchen in Bewegung sieht findest du | <small>Ein Film, bei dem man die Teilchen in Bewegung sieht, findest du [http://www.youtube.com/watch?v=KE8OEMlPcCA hier].</small> | ||
</div> | </div> | ||
</div> | </div> | ||
Aufgrund der Definition der Dichte können wir nun erklären, warum die Dichte dann geringer ist: | Aufgrund der Definition der Dichte können wir nun erklären, warum die Dichte dann geringer ist: | ||
:''Die Dichte ist ja Masse pro Volumen. Wenn die '''Masse gleich bleibt''' (''gleich viele Teilchen'') aber '''das Volumen zunimmt''' (''wegen dem Abstand zwischen den Teilchen'') dann wird die Dichte beim Erhitzen immer geringer.'' | |||
==== Warum ist die Dichteanomalie für uns wichtig? ==== | Warum das nun beim Wasser tatsächlich anders ist, lässt sich mit diesem einfachen Teilchenmodell nicht erklären. Tatsächlich ist es der Abstand der Wasser-Teilchen, der im gefrorenen Zustand größer ist als in der Flüssigkeit. | ||
Und da unterscheidet sich das Wasser von allen anderen Stoffen, weil Eis eine geringere Dichte als das flüssige Wasser hat. Man spricht deshalb von der '''''Dichteanomalie des Wassers'''''. | |||
====Warum ist die Dichteanomalie für uns wichtig?==== | |||
<div class="grid"> | <div class="grid"> | ||
<div class="width-1-2">Die Tatsache, dass gefrorenes Wasser, also Eis, nicht absinkt ist von wesentlicher Bedeutung für das Überleben auf der Erde. Denn nur so können im Winter die Wasserbewohner überleben. Denn ist das Wasser tief genug, so friert ein Gewässer nicht durch und unten bildet sich eine 4°C kalte Schicht, in der die Wasserbewohner überleben können.</div> | <div class="width-1-2">Die Tatsache, dass gefrorenes Wasser, also Eis, nicht absinkt ist von wesentlicher Bedeutung für das Überleben auf der Erde. Denn nur so können im Winter die Wasserbewohner überleben. Denn ist das Wasser tief genug, so friert ein Gewässer nicht durch und unten bildet sich eine 4°C kalte Schicht, in der die Wasserbewohner überleben können.</div> | ||
<div class="width-1-2">[[File:Anomalous expansion of water Summer Winter.svg]]</div> | <div class="width-1-2">[[File:Anomalous expansion of water Summer Winter.svg]]</div> | ||
</div> | </div> | ||
[[Kategorie:Dichte]] | [[Kategorie:Dichte]] | ||
[[Kategorie:Stoffeigenschaft]] | [[Kategorie:Stoffeigenschaft]] | ||
[[Kategorie: | [[Kategorie:Metalle]] | ||
[[Kategorie: | [[Kategorie:Chemie]] | ||
Aktuelle Version vom 14. Mai 2022, 03:20 Uhr
Worum geht es hier
Wenn etwas im Wasser untergeht sagt man gerne "das war zu schwer". Aber, was ist mit ganzen Baumstämmen? Sind die leicht, weil sie nicht untergehen? Nein, das kann es nicht sein, denn sicher ist ein großer Baumstamm nicht gerade leicht. Und dann geht ja selbst der leichteste Stein im Wasser unter.
Also, damit es ist ganz klar, dass das Gewicht nicht die Eigenschaft sein kann, weswegen etwas schwimmt oder eben untergeht.
Woran liegt es also?
Zunächst einmal sollte man, damit man zwei Stoffe wirklich vergleichen kann, die gleiche Menge davon nehmen. Denn es ist klar, dass wenn man ein große Portion von einem Stoff hat, diese Portion natürlich auch schwerer ist als eine kleinere.
Betrachten wir also kleine Würfelchen mit der Seitenlänge von 1 cm, die damit alle das gleiche Volumen von 1cm³ haben. Wiegt man diese Würfel, so stellt man fest, dass die Würfel aus verschiedenen Materialien alle unterschiedlichen Massen haben.
| Stoff | Masse von 1 cm³ |
|---|---|
| Eisen | 7,874 g/cm³ |
| Aluminium | 2,6989 g/cm³ |
| Blei | 11,342 g/cm³ |
| Holz (je nach Holzart) |
z.B. zwischen 0,47 g/cm³ (Fichte) und 0,69 g/cm³ (Esche) |
| Kunststoff (z.B.Poylethylen) |
zwischen 0,915 g/cm³ und 0,97 g/cm³ |
| usw. | ... |
So zeigt sich deutlich, dass 1 cm³ von Holz wesentlich leichter sind, als etwa 1 cm³ Eisen. Die gleiche Menge an Holz ist also leichter als die entsprechende Menge an Eisen.
Da man von einem Stoff nicht immer ein 1 cm³-Würfelchen zur Hand hat, müsste man die Masse eines Stoffes mit seinem Volumen vergleichen. Berechnet man den Quotienten aus Masse und Volumen, so erhält man eine Zahl die man als DICHTE bezeichnet.
oder mit Symbolen .
Einheit der Dichte: bei Feststoffen und Flüssigkeiten oder bei gasförmigen Stoffen- Bei dem "komischen Buchstaben , der fast wie ein "p" aussieht, handelt es sich um einen griechischen Buchstaben, wie ihr sie auch von der Winkelbenennung kennt. Hier ist es das kleine "rho" (lies: roh).
Die DICHTE (oder auch spezifisches Gewicht) ist eine Stoffeigenschaft, die für viele reine Stoffe genau bestimmt werden kann. Daher kann man die Dichte auch nutzen, um einen Stoff zu identifizieren. Damit man nicht immer selber die Dichte berechnen muss, gibt es die Werte von ganz vielen Stoffen in Datensammlungen, in denen du nachschlagen kannst. In der Wikipedia findest du zu fast jedem Stoff, der dort aufgeführt ist, immer auch die Dichte, da es eine wichtige Stoffeigenschaft ist. Schul-Bücher enthalten meist eine Liste der Elemente mit Eigenschaften, in denen meist auch die Dichten angegeben sind. Einen Überblick liefern die Tabellen hier:
Die Dichte eines Stoffes kann schon helfen, einen Stoff zu identifizieren, daher sollte man auch wissen, wie man die Dichte bei verschiedenen Stoffen bestimmen kann.
Praktische Bestimmung von Dichten
Für die Bestimmung der Dichte eines unbekannten Stoffes muss man eine Portion des reinen Stoffes haben und von dieser Portion das Volumen und sein Gewicht bestimmen. Je nachdem, in welchem Aggregatzustand der Stoff vorliegt, führt das zu unterschiedlichen Problemen bei der Bestimmung der beiden Werte.
Zum einen, die Bestimmung des Volumens: Nicht immer sind Stoffe in praktischen Würfeln oder Quadern gegeben. Bei solchen Würfeln könnte man einfach die Kantenlänge messen und das Volumen daraus berechnen.
- Volumen eines Würfels mit der Seitenlänge a:
- Volumen eines Quaders mit den Seitenlängen a, b, c:
Was aber bei unregelmäßigen Körpern machen, wie etwa einem Stein? Hier kann man das Volumen mit einem Lineal nur grob schätzen. Auch bei Flüssigkeiten ist die Volumen-Bestimmung mit Hilfe eines Quaders unpraktikabel, wobei man da ja Messzylinder hat, mit denen man das Volumen einer Flüssigkeitsportion bestimmen kann. Bei Gasen geht das dann aber auch wieder nicht, denn ein Gas muss rundherum eingeschlossen sein, weil es sich sonst verflüchtigt.
Diese Überlegungen zeigen die "Probleme", die es nötig machen, für jeden Aggregatzustand ein spezielles Verfahren zu nutzen, mit denen man das Volumen und die Masse von einer Stoffportion bestimmen kann, um dann die Dichte zu berechnen.
- Experiment und Aufgaben zur Dichtebestimmung bei Feststoffen
- Experiment und Aufgaben zur Dichtebestimmung bei Flüssigkeiten
- Experiment und Aufgaben zur Dichtebestimmung bei Gasen
Aufgaben und Berechnungen mit der Dichte
Die Dichte ist nicht nur ein Wert, denn man bestimmt, um einen Stoff zu identifizieren. Auch bei bekannter Dichte, gibt es da zahlreiche Anwendungen, wo mit Hilfe der Dichte etwas berechnet werden kann. Hier ein paar schnelle Beispiele:
- Welches Volumen hat eine angegebene Masse z.B. von Öl? Das wäre interessant wenn man keine Waage hat, aber ein genaues Messgefäß für das Volumen.
- Umgekehrt kann man bei bekannter Dichte, von der Masse einer Stoffportion auf das Volumen schließen.
- Auch die Berechung der Dichte wäre interessant, wenn man zum Beispiel untersuchen will, ob der Gold-Ring wirklich komplett aus Gold ist oder nur vergoldet.
Auf der folgenden Unterseite geht es um solche Aufgaben und du erhältst alle Informationen, wie man die Formel für die Defintion der Dichte nutzen kann, um alles zu berechnen.
→ Stöchiometrie - Berechnungen mit der Dichte
Bedeutung der Dichte für den Auftrieb
Das Bild rechts zeigt verschiedene flüssige und feste Stoffe übereinander. Von oben nach unten sind es:
- Benzin, rot angefärbter Reinigungsalkohol (Isopropanol), Speise-Öl, Wachs, blau gefärbtes Wasser, Aluminium
Was hat das mit der Dichte zu tun?
Dazu müsste man sich die Dichte-Werte zusammensuchen und die Zahlen miteinander vergleichen.
| Stoff | Dichte |
|---|---|
| Benzin | 0,748 g/cm³ |
| Isopropanol | 0,78 g/cm³ |
| Speise-Öl | 0,91 g/cm³ |
| Wachs | 0,95 g/cm³ |
| Wasser | 1 g/cm³ |
| Aluminium | 2,6989 g/cm³ |
Du wirst erkannt haben, dass die Dichte von oben nach unten immer mehr zunimmt.
Flüssige Stoffe ordnen sich in einem Gefäß immer so an, dass der Stoff mit der geringsten Dichte am weitesten oben ist.
Feste Stoffe können in einer Flüssigkeit ...
- an der Oberfläche schwimmen ... wenn die Dichte vom Feststoff geringer als die Dichte der Flüssigkeit ist.
- in der Flüssigkeit schweben ... wenn die Dichte vom Feststoff gleich der Dichte der Flüssigkeit ist.
- auf den Boden sinken ... wenn die Dichte vom Feststoff größer als die Dichte der Flüssigkeit ist.
Dies gilt natürlich nur, wenn die Stoffe sich nicht vermischen oder ineinander löslich sind.
Gleiches gilt auch für die Fettaugen auf der Suppe. Vergleicht man nämlich Wasser und Öl, so hat Öl die geringere Dichte.
Dies gilt übrigens nicht nur in Flüssgikeit sondern auch in der Luft. Habe Stoffe ungefähr die gleiche Form, so lassen sich Stoffe mit geringer Dichte leichter wegpusten und fallen weniger langsam runter.
Wissenwertes rund um die Dichte
Nach den schon vorher angesprochenen Beispielen, wie sich die Dichte auswirkt, noch ein paar weitere alltägliche Effekte, wo wir die Dichte zu spüren bekommen.
Leicht- und Schwermetall
Den Begriff Schwermetalle wirst du vielleicht schon mal gehört haben. Meist wird er im Zusammenhang mit Umweltverschmutzung genannt. Schwermetall-Verbindungen sind meist für den Menschen und Tiere ungesund. Man kann sie allerdings nicht so einfach sehen, die Schwermetall-Verbindungen sind Salzartige Stoffe, die im Wasser löslich sind.
Was das mit der Dichte zu tun hat?
Die Dichte hat zum dabei durchaus eine besondere Bedeutung. So hat zum Beispiel die recht hohe Dichte von Blei![]() (11,342 g/cm³) durchaus praktische Anwendungen.
(11,342 g/cm³) durchaus praktische Anwendungen.
Es wird als Gewicht verwendet (Bleigürtel beim Tauchen, Bleiband bei Gardinen) und die schweren Bleischürzen schirmen aufgrund der hohen Dichte auch gut gegen radioaktive Strahlen ab, weswegen sie beim Röntgen eingesetzt werden. Es gibt zwar noch bessere, weil dichtere Metalle, aber die sind zu teuer.
Auch Gold![]() hat eine recht hohe Dichte. Und gerade Quecksilber
hat eine recht hohe Dichte. Und gerade Quecksilber![]() überrascht mit seiner hohen Dichte für eine Flüssigkeit, wenn man das erste Mal eine Quecksilber-Flasche hochhebt.
überrascht mit seiner hohen Dichte für eine Flüssigkeit, wenn man das erste Mal eine Quecksilber-Flasche hochhebt.
Dagegen nutzt man die Leichtmetalle wie Magnesium![]() und Aluminium
und Aluminium![]() zum Beispiel beim Fahrzeugbau um Gewicht und damit Treibstoff zu sparen.
zum Beispiel beim Fahrzeugbau um Gewicht und damit Treibstoff zu sparen.
Die Dichteanomalie des Wassers
Die Dichte von Wasser ist unnormal!? Das erscheint dir sicher irgendwie merkwürdig, denn Wasser ist ein so alltäglicher Stoff ... wäre einem da etwas Unnormales nicht schon aufgefallen?
Dabei können wir froh sein, dass die Dichte des Wassers, bzw. des festen Wassers also Eis, sich so anders verhält als andere Stoffen. Um besser zu verstehen, was beim Wasser so unnormal ist, solltest du dir diesen Film anschauen:
Folgendes ist zu erkennen:
- Feste Wachsklumpen gehen in flüssigem Wachs unter → die Dichte von festem Wachs ist geringer als die Dichte von flüssigem Wachs
- Gefrorener Eiseissig (= hochkonzentrieter Essig) geht im flüssigen Eisessig ebenfalls unter → die Dichte von festem Eisessig ist geringer als die Dichte von flüssigem Eissessig
- Gefrorenes Wasser, also Eis, schwimmt im flüssigen Wasser → die Dichte von festem Wasser (= Eis) ist höher als die Dichte von flüssigem Wasser
Wachs und Eisessig sind hier die eigentlich normalen Stoffe. Denn bei allen anderen Stoffen, eben außer dem Wasser, ist es so, dass der feste Stoff in seinen flüssigen Aggregatzustand untergeht. Und das ist das Unnormale am Wasser.
Wenn man hier mal den Begriff "Dichte" nutzt kann man also sagen.
Wie lässt sich das erklären, dass diese Verhalten normal ist? Im Grunde genommen geht das ganz einfach: dazu müssen wir nur die kleinsten Teilchen von Stoffen betrachten. In dem folgenden Video siehst du eine Simulation eines beliebigen Stoffes und dessen Teilchen bei verschiedenen Temperaturen.
Sortieren wir nun die Beobachtungen ein wenig, indem wir das Teilchenmodell des Stoffes mal in drei einzelnen Bildern betrachten, je eines für jeden Aggregatzustand.
Bei sehr niedrigen Temperaturen ist der Stoff fest und die Bewegung der Teilchen ist sehr langsam. Die Teilchen sind ganz nah beieinander und eng gepackt.
Einen Film, bei dem man die Teilchen in Bewegung sieht, findest du hier.
Bei mittleren Temperaturen ist der Stoff flüssig und die Teilchen sind zwar auch noch nah beieinander, da sich aber die Teilchen mit dem Erhitzen des Stoffes schneller bewegen, können sie nicht mehr so eng zusammen bleiben, wie vorher beim festen Stoff. Der von den Teilchen eingenommene Platz ist daher größer.
Ein Film, bei dem man die Teilchen in Bewegung sieht, findest du hier.
Bei sehr hohen Temperaturen ist der Stoff gasförmig und die Teilchen sind noch schneller und daher wird ihr Abstand noch größer und die Teilchen sind weit im Raum verteilt.
Ein Film, bei dem man die Teilchen in Bewegung sieht, findest du hier.
Aufgrund der Definition der Dichte können wir nun erklären, warum die Dichte dann geringer ist:
- Die Dichte ist ja Masse pro Volumen. Wenn die Masse gleich bleibt (gleich viele Teilchen) aber das Volumen zunimmt (wegen dem Abstand zwischen den Teilchen) dann wird die Dichte beim Erhitzen immer geringer.
Warum das nun beim Wasser tatsächlich anders ist, lässt sich mit diesem einfachen Teilchenmodell nicht erklären. Tatsächlich ist es der Abstand der Wasser-Teilchen, der im gefrorenen Zustand größer ist als in der Flüssigkeit. Und da unterscheidet sich das Wasser von allen anderen Stoffen, weil Eis eine geringere Dichte als das flüssige Wasser hat. Man spricht deshalb von der Dichteanomalie des Wassers.