Oberstufen-Chemiebuch Kontextorientiert/Alltags-Kunststoffe - Kohlenstoff-Ketten in viele Variationen
Nachdem auf der vorherigen Seiet vor allem mit den Prinzipien der Kunststoffchemie beschäftigt haben, soll es nun um konkrete Typen an Kunststoffen gehen mit verschiedenen Monomeren und Polymeren. Dabei werden wir dann die Theorie nutzen, um die Eigenschaften der Stoffe erklären zu können bzw. selber bestimmen können.
Polyethylen
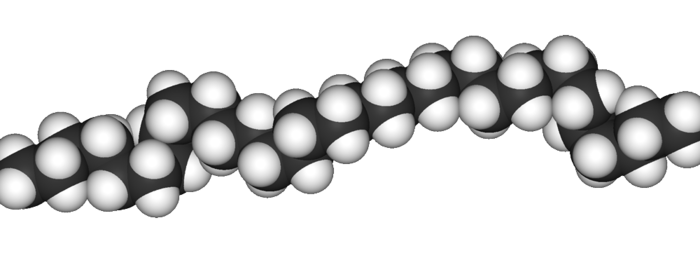
Das Polyethylen (kurz PE) ist zwar nicht das erste Polymer, dass hergestellt wurde, aber es ist das Einfachste. Der Name Polyethylen ergibt sich aus dem Ausgangsstoff, dem Monomer, hier also das Ethylen = Ethen. Es ist deshalb das einfachste, da an der grundlegenden Struktur, die für eine Polymerisationsreaktion notwendig ist, also der Doppelbindung, keine weitere Kette oder Gruppe hängt.
Polyethylen ist mit einem Anteil von ca. 38 Prozent der weltweit am meisten genutzte Kunststoff. Die Anwendungen sind vielfältig:
Geschichtliche Entwicklung
Zum ersten Mal wurde 1898 von dem deutschen Chemiker Hans von Pechmann zufällig hergestellt, als er mit Diazomethan (siehe Bild) experimentierte. Man erhielt eine weiße, wachsartige Substanz. Die Entstehung lässt sich recht leicht erklären, denn wenn vom instabilen Diazomethan ein Stickstoff-Molekül abgespalten wird, werden CH2-Gruppen frei, die sich zu einer langen Kette zusammensetzen können. Da Diazomethan sehr instabil ist, deswegen nicht in größeren Mengen gelagert werden kann und nebenbei auch giftig ist, ist die Herstellungsweise wenig erfolgreich gewesen.
Die erste industrielle Polyethylen-Synthese wurde (wieder durch Zufall) 1933 in England von Chemikern entdeckt, die für die ICI (Imperial Chemical Industries) arbeiteten. Bei extrem hohen Drücken (ca. 1400 bar) erzeugten sie aus einem Gemisch aus Ethylen und Benzaldehyd ein weißes, wachsartiges Material. Das Benzaldehyd ist für die Reaktion nicht wirklich von Bedeutung und tatsächlich funktionierte die Methode nur wegen kleinen Mengen an Sauerstoff, die ins Reaktionsgefäß gelangt waren. Zwei Jahre später konnte dann aber wieder ein Chemiker von ICI eine tatsächlich funktionierende und nachvollziehbare Hochdrucksynthese für Polyethylen vorstellen. Sie war die Grundlage für die industrielle Produktion am 1939.
Ein weiterer Meilenstein in der industriellen Herstellung von Polyethylen war die Entwicklung von Katalysatoren, die die Polymerisation bei milden Temperaturen und Drücken ermöglichen. Immer noch verwendet wird der 1953 nach seinen Entdeckern (Karl Ziegler und Giulio Natta) benannte Ziegler-Natta-Katalysator, der Titanhalogeniden und aluminiumorganischen Verbindungen enthält.
Verschiedene Typen von Polyethylen
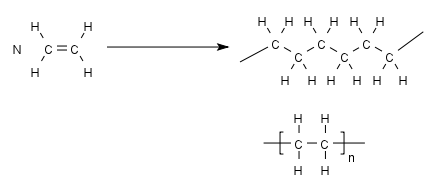
Rein theoretisch ist eine solche Polymerisation ja eine eindeutige Sache:
- mit einer Startreaktion wird eine Doppelbindung (hier am Ethylen) aufgespalten und damit die Kettenreaktion vorbereitet
- in der Kettenreaktion bindet sich immer wieder eine C2H4-Gruppe nach der anderen, so dass die Kette länger und länger wird.
Natürlich wird nicht nur an einer Stelle gestartet, aber wir gehen zunächst einmal davon aus, dass jede einzlene Kettenverlängerung für sich abläuft. Tatsächlich ist es so, das bei den ersten Polyethylen-Synthesen, aufgrund hohen Temperaturen gar keine so geordnete Polymerisation stattgefunden hat. Stattdessen kann man sagen, das die hohen Temperaturen an ganz vielen Stellen gleichzeitig die Doppelbindungen aufbrechen, dabei Radikale entstehen und so gleichzeitig viele Ketten anfangen zu wachsen. Diese radikalischen Ketten könnten sich dann beliebig mit anderen Ketten verbinden und durch Umlagerungen innerhalb des Ketten-Moleküls kann auch eine Seitenkette an einer längeren angehängt werden. Tatsache ist, dass die ersten Polyethlene sehr stark verzweigte Ketten bildeten, die man sich so vorstellen kann:
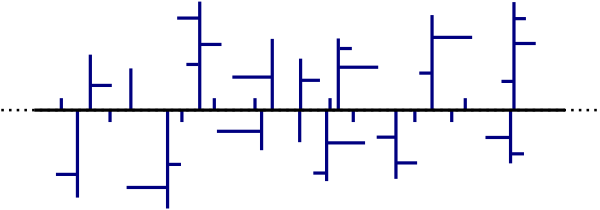
Die ersten Polyethylene die hergestellt wurden waren eher klebrige, wachsartige Produkte und keinesfalls fest.
- Was lässt sich damit über die allgemeinen physikalischen Eigenschaften des Polymers vermuten?
Führt man stattdessen die Polymerisation bei niedrigen Temperaturen durch, wie es zum Beispiel beim Ziegler-Natta-Katalysator der Fall ist, so kann man den Verzweigungsgrad genau bestimmen. Für die Entdeckungen zur Nutzung von Katalysatoren bei der Polymerisation bekamen Karl Ziegler und Giulio Natta 1963 den Nobelpreis für Chemie.
Statt der stark verzweigten Struktur, ist mit dem Katalysator nun möglich auch wenig bis gar nicht verzweigte Polyethylensorten zu gewinnen.
| PE-HD oder HDPE | |
| PE-LLD oder LLDPE | |
| PE-LD oder LDPE | 
|
Die verschiedenen Kürzel, die hinter den Buchstaben PE stehen, beschreiben den wesentlichen Unterschied zwischen den drei Sorten, nämlich die unterschiedliche Dichte:
- PE-HD hat einen hohe Dichte (High Density) von durchschnittlich etwa 0,955 g/cm3
- PE-LD hat eine geringe Dichte (Low Density) von durchschnittlich etwa 0,925 g/cm3
- PE-LLD hat eine teilweise recht niedrige Dichte von 0,87–0,94 g/cm3, der Namen leitet sich von Linear Low Density ab, da trotz der wenig verzweigten Struktur eine niedrige Dichte hat.
Schauen wir uns zur Wiederholung nach einmal den Begriff der Dichte an:
- Wie ist die Dichte definiert?
- Vergleicht man die Dichte von Stoffen im gasförmigen bzw. festen Zustand, so hat man gasförmigen Zustand eine sehr viel geringere Dichte? Wie lässt sich das erklären?
- Wie kann man bei verschiedenen Feststoffen unterschiedliche Dichten erklären?
Hier hat man einen direkten Zusammenhang zwischen innerer Struktur und der von außen zu messenden Eigenschaft, hier der Dichte. Dichte gibt ja an, wieviel Masse auf ein bestimmtes Volumen kommt. Da wir hier die gleichen Arten an Atomen (nur C und H) und eigentlich den gleichen Aufbau haben, geht es letztendlich hier um die Anzahl der Atome, die sich in einem Raumbereich befinden. Und die hängt von dem inneren Aufbau ab. Man kann sich das so vorstellen, dass bei unverzweigten Ketten, wie beim PE-HD, diese Ketten sehr nah aneinander und parallel anlagern können, da nichts absteht. Damit liegen viele Atome näher beieinander und damit ist mehr Masse im gleichen Raumbereich vorhanden.
Beim PE-LD und PE-LLD ist der Abstand offensichtlich größer (also weniger Atome pro Raumbereich), was sich damit erklären lässt, dass die Seitenketten dazu führen, dass die Ketten ungeordnet neben- bzw. durcheinanderliegen.
Interessanterweise die Dichte bei PE-LLD teilweise sogar niedriger als bei dem PE-LD. Das passt ja irgendwie gar nicht zu dem Aufbau der Kohlenstoffkette und der Menge an Verzweigungen. Spekuliere darüber, wie man das erklären könnte!
Zusammenhang zwischen Struktur und Eigenschaften genauer betrachtet
Wie auch die Dichte lassen sich weitere Eigenschaften der verschiedenen PE-Typen aufgrund des unterschiedlichen Molekülbaus erklären. Betrachten wir eine anderes andere Auswirkung, zu der wir bisher nur die Bezeichnung angesprochen haben. Dazu noch einmal kurz als Wiederholung:
Wie sich der unterschiedliche Molekülaufbau auf den Anteil an kristallinen Bereichen auswirkt kann man an der folgenden Tabelle auslesen. Dazu noch einmal die genauen Daten zur Dichte im Vergleich:
| Eigenschaft | PE-LD | PE-HD | PE-LLD |
|---|---|---|---|
| Dichte in g/cm3 | 0,915–0,935 | 0,94–0,97 | 0,87–0,94 |
| Kristallinität in % | 40–50 | 60–80 | 10–50 |
Kristalline Bereiche bedeuten ja, dass die Molekülketten parallel liegen und somit wenig Platz einnehmen und damit passen diese Daten gut zu der Dichte der verschiedenen Polyethylen-Typen.
Betrachten wir nun mal die Schmelz- und Siedetempertaur der verschiedenen PE-Typen. Es sind ja allgemein zwei Dinge, die im Wesentlichen bei der Siedetemperatur eine Rolle dabei spielen:
- Die Masse der Teilchen, die beim Erwärmen in Bewegung gebracht werden müssen.. Je größer die Masse der Teilchen ist, desto schwieriger ist es, sie in Bewegung zu bringen. Bei den Kunststoffen haben wir allgemein sehr große Moleküle (bis zu mehreren tausend C-Atomen lange Ketten!), so dass es hier vor allem darum geht, die Ketten in beim Schmelzen in Bewegung zu bringen. Diese langen Ketten führen auch dazu, dass die Kunststoffe meist fest sind.
- Die Anziehung der Moleküle untereinander, die überwunden werden muss. Damit sich die Moleküle bewegen können, müssen auch die Anzeihungskräfte der Moleküle/Molekülketten untereinander überwunden werden. Da wir bei PE reine Kohlenwasserstoffketten haben, haben wir keine polaren Gruppierungen und daher wirken nur die Van-der-Waals-Kräfte.
Die Molekular-Masse spielt nur dann eine Rolle, wenn sich die Anzahl der Atome in einer Polymer-Kette wesentlich unterschiedet. Bei festen Werkstoffen es weniger wichtig, denn die Unterschiede sind nicht so groß. Liegen die Ketten aber parallel (wie in den teilkristallinen Bereichen), so können die Van-der-Waals-Kräfte besser wirken. Die Van-der-Waals-Kräfte bezeichnet ja die Anziehung durch sich zufällig ergebende Dipole, die bei günstiger Lage an Nachbarmoleküle weitergegeben werden können (temporäre und induzierte Dipole), wodurch kurzfristig eine Anziehung besteht. Die Anziehung ist umso höher, je größer die Fläche ist und je paralleler die Moleküle liegen.
Wenn die Anziehung bei parallelen Ketten größer ist, sollte auch die Siedetemperatur mit höherer Kristallität größer sein. Hier dazu die Daten, die das belegen:
| Eigenschaft | PE-LD | PE-HD | PE-LLD |
|---|---|---|---|
| Kristallinität in % | 40–50 | 60–80 | 10–50 |
| Schmelzpunkt in °C | 130–145 | 130–145 | 45–125 |
| Wärmeformbeständigkeit bis °C | 80 | 100 | 30–90 |
Offensichtlich passt der Zusammenhang bei dem PE-LLD sehr gut, denn es hat die niedrigste Siedetemperatur bei dem geringsten Anteil an Kristallinität. Das PE-LD zeigt, ähnlich wie bei der Dichte, dass es da Auswirkungen durch die langen und auch verzweigten Seitenketten gibt, die die Anziehung wiederum verbessern, so dass wir bei PE-HD und PE-LD den gleichen Schmelzbereich haben.
Unterschiede gibt es bei der Wärmeformbeständigkeit, einer Messgröße zur Untersuchung von Kunststoffen.
Allerdings bleibt das PE-HD länger stabil und ist erst bei einer höheren Temperatur verformbar.
Das folgende Bild zeigt noch einmal einen Überblick, wie Molekülmasse und Kristallinität sich auf die Eigenschaften der Polyethylene als Feststoff auswirken. Neben den der Schmelztemperatur gibt es da noch Unterschiede bezüglich der Festigkeit (hart, weich, spröde).
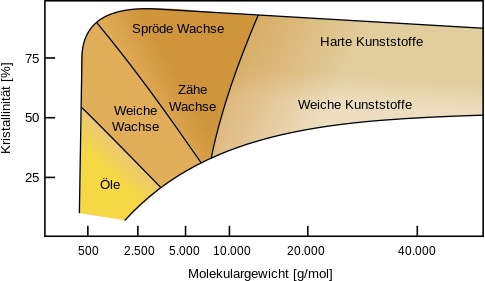
Harte Kunststoffe bekommt man also allgemein nur, wenn es einen hohen Zusammenhalt zwischen verschiedenen Molekülketten gibt. Das kann entweder durch Kristalline Bereiche geschehen oder, was wir bisher nur theoretischen angesprochen haben, bei den Duroplasten, wo man echte Bindungen zwischen den Molekülketten haben muss.
Versuche die folgende Aussagen zu begründen:
Schauen wir uns noch die chemische Beständigkeit und die Stabilität an in einer Tabelle an:
| Eigenschaft | PE-LD | PE-HD | PE-LLD |
|---|---|---|---|
| Chemische Beständigkeit | bedingt beständig, außer gegen starke Oxidationsmittel | beständig, außer starke Oxidationsmittel | bedingt beständig |
| Dehnung an der Streckgrenze in % | 20 | 12 | 16 |
Vervollständige den Multpile-Choice-Test zu chemischen Beständigkeit:
Recycling von Polyethylen
Wie andere Kunststoffe geht man davon aus, dass auch Polyethylen sich in der Natur nichts wirklich abbaut.
Abschluss
Obwohl wir uns hier nur mit einer Art Kunststoff beschäftigt haben, zeigt sich schon hier, das durch die Wahl eines Produktionsverfahren, Produktionsbedingungen, Katalysatoren usw. gezielt Polymere mit erwünschten Eigenschaften hergestellt werden können. Und neben harten oder weichen Kunststoffen sind auch Wachse, Fette und sogar Öle aus Polyethylen herstellbar.
Was wir beim Polyethylen schon erkannt haben, werden wir auch bei den folgenden Kunststoffe anwenden ... und noch ein wenig mehr kennenzulernen.
Polypropylen (PP)
Polyvinylchlorid (PVC)
Polystyrol (PS)
Besser bekannt in geschäumtem Zustand als Styropor® (Handelsname der BASF)
Polytetrafluorethylen (PTFE)
Sein Handelsname ist Teflon® (E. l. Du Pont de Nemours and Company) oder Tefal®
Polymethylmethacrylat (PMMA)
Unter dem Handelsnamen Plexiglas® (Evonik Industries AG) verkauft.
Polyacrylnitril (PAN)
, als Copolymer mit Polymethylmethacrylat zur Herstellung von Textilfasern