Chemie-Buch I zum Lehrplan in Rheinland-Pfalz/Chemie - die Wissenschaft von den Stoffen: Unterschied zwischen den Versionen
Markierung: 2017-Quelltext-Bearbeitung |
Markierung: 2017-Quelltext-Bearbeitung |
||
| Zeile 167: | Zeile 167: | ||
{{Box|VERSUCH 1 - Verhalten beim Erhitzen|2= | {{Box|VERSUCH 1 - Verhalten beim Erhitzen|2= | ||
'''Durchführung:''' Holt euch ein gebrauchtes Reagenzglas vom Lehrertisch. Gebt mit einem Spatel nicht mehr als 1 cm eures Stoffes in das gebrauchte Reagenzglas und erhitzt es über dem Bunsenbrenner. '''Achtet auf die besprochenenen Sicherheitsmaßnahmen'''. Erhitzt wie auch beim Wasser erst vorsichtig und wenn nichts passiert stärker. Allerdings muss das Reagenzglas nicht geschmolzen werden, um sagen zu können, dass der Stoff sich beim Erhitzen nicht verändert. | {{Sicherheitsinfo|Schutzbrille}}'''Durchführung:''' Holt euch ein gebrauchtes Reagenzglas vom Lehrertisch. Gebt mit einem Spatel nicht mehr als 1 cm eures Stoffes in das gebrauchte Reagenzglas und erhitzt es über dem Bunsenbrenner. '''Achtet auf die besprochenenen Sicherheitsmaßnahmen'''. Erhitzt wie auch beim Wasser erst vorsichtig und wenn nichts passiert stärker. Allerdings muss das Reagenzglas nicht geschmolzen werden, um sagen zu können, dass der Stoff sich beim Erhitzen nicht verändert. | ||
'''Entsorgung:''' Versucht nach dem Abkühlen den Inhalt auszuschütten. Wenn das geht und Reste im Reagenzglas übrig bleiben, bitte gut mit Wasser und einer Bürste ausspülen. Kann der Inhalt nicht entfernt werden, bitte das Reagenzglas vorzeigen, damit ich entscheiden kann, ob es sinnvoll ist, es wegzuwerfen. | '''Entsorgung:''' Versucht nach dem Abkühlen den Inhalt auszuschütten. Wenn das geht und Reste im Reagenzglas übrig bleiben, bitte gut mit Wasser und einer Bürste ausspülen. Kann der Inhalt nicht entfernt werden, bitte das Reagenzglas vorzeigen, damit ich entscheiden kann, ob es sinnvoll ist, es wegzuwerfen. | ||
| Zeile 189: | Zeile 189: | ||
{{ | {{Box|VERSUCH 3 - pH-Wert der Lösung| | ||
{{Sicherheitsinfo|Händewaschen}} | |||
:''Das Experiment sollte immer nach dem Experiment Nr. 2 durchgeführt werden! Führt deshalb erst Nr. 2 durch und dann Nr. 3. Bringt also diese Anleitung erst noch einmal zurück, wenn ihr Nr. 2 noch nicht durchgeführt habt.'' | :''Das Experiment sollte immer nach dem Experiment Nr. 2 durchgeführt werden! Führt deshalb erst Nr. 2 durch und dann Nr. 3. Bringt also diese Anleitung erst noch einmal zurück, wenn ihr Nr. 2 noch nicht durchgeführt habt.'' | ||
'''Durchführung:''' Holt euch ein weiteres sauberes Reagenzglas, gebt soviel destilliertes Wasser wie im anderen Reagenzglas aus Experiment Nr. 2 hinein. Stellt die beiden Reagenzgläser nebeneinander in den Reagenzglasständer. Gebt nun vom sogenannte Universalindiktor in die Reagenzgläser, und zwar in beide gleich viele Tropfen. Die Farbe des Wasser | '''Durchführung:''' Holt euch ein weiteres sauberes Reagenzglas, gebt soviel destilliertes Wasser wie im anderen Reagenzglas aus Experiment Nr. 2 hinein. Stellt die beiden Reagenzgläser nebeneinander in den Reagenzglasständer. Gebt nun vom sogenannte Universalindiktor in die Reagenzgläser, und zwar in beide gleich viele Tropfen. Die Farbe des Wasser dient als Vergleichslösung, um die Färbung der Lösung beurteilen zu können. Ist die Farbe der Lösung ... | ||
* wie beim Wasser, ist die Lösung '''neutral'''. | * wie beim Wasser, ist die Lösung '''neutral'''. | ||
* rötlich, so ist die Lösung '''sauer'''. | * rötlich, so ist die Lösung '''sauer'''. | ||
* bläulich, so ist die Lösung '''alkalisch''' | * bläulich, so ist die Lösung '''alkalisch''' | ||
{{Lösung versteckt|1= | |||
Der pH-Wert ist ein Zahl, mit der eine bestimmte Eigenschaften einer Lösung beschrieben wird. | Der pH-Wert ist ein Zahl, mit der eine bestimmte Eigenschaften einer Lösung beschrieben wird. | ||
* Wasser hat den '''pH-Wert 7''' und wird als '''neutral''' bezeichnet. | * Wasser hat den '''pH-Wert 7''' und wird als '''neutral''' bezeichnet. | ||
* Eine '''saure Lösung''' hat einen '''pH-Wert von 0 bis 7''', wobei 0 sehr sauer ist und z.B. 6 nur ein wenig sauer ist. Sauer ist hier gleichbedeutend mit "schmeckt sauer". | * Eine '''saure Lösung''' hat einen '''pH-Wert von 0 bis 7''', wobei 0 sehr sauer ist und z.B. 6 nur ein wenig sauer ist. Sauer ist hier gleichbedeutend mit "schmeckt sauer". | ||
* Eine '''alkalische Lösung (Lauge)''' hat einen pH-Wert von 7 bis 14, wobei 8 ein wenig alkalisch und 14 sehr alkalisch ist. Alkalische Lösungen lassen sich auch am Geschmack erkennen, aber es schmeckt wie Seife. Bekannt sind Seifenlauge und Laugenbrezel. | * Eine '''alkalische Lösung (Lauge)''' hat einen pH-Wert von 7 bis 14, wobei 8 ein wenig alkalisch und 14 sehr alkalisch ist. Alkalische Lösungen lassen sich auch am Geschmack erkennen, aber es schmeckt wie Seife. Bekannt sind Seifenlauge und Laugenbrezel. |2=Zeige Informationen zum pH-Wert|3=Verberge Informationen}} | ||
'''Entsorgung:''' In den Abfluss gießen, Reagenzgläser und Waschbecken gut mit Wasser ausspülen. | '''Entsorgung:''' In den Abfluss gießen, Reagenzgläser und Waschbecken gut mit Wasser ausspülen. | ||
| Zeile 208: | Zeile 208: | ||
{{ | {{Box|VERSUCH 4 - Betrachtung unter dem Mikroskop| | ||
'''Durchführung:''' Gebt ganz wenige Körnchen eures Stoffes auf eines der gelben Scheiben und stellt dann die Mikroskop-Kamera darüber eventuell kann man an dem großen, silbernen Drehrad an der Kamera das Bild etwas schärfer stellen. Beschreibt, was ihr seht: | '''Durchführung:''' Gebt ganz wenige Körnchen eures Stoffes auf eines der gelben Scheiben und stellt dann die Mikroskop-Kamera darüber eventuell kann man an dem großen, silbernen Drehrad an der Kamera das Bild etwas schärfer stellen. Beschreibt, was ihr seht: | ||
* Kann man an verschiedenen Körnchen immer wieder die gleiche Form erkennen und haben die Körnchen glatte Flächen, so hat man '''Kristalle'''. | * Kann man an verschiedenen Körnchen immer wieder die gleiche Form erkennen und haben die Körnchen glatte Flächen, so hat man '''Kristalle'''. | ||
| Zeile 219: | Zeile 219: | ||
{{ | {{Box|VERSUCH 5 - Verhalten bei Zugabe von Säure| | ||
'''Durchführung:''' Gebt etwa 0,5 cm eures Stoffes in ein sauberes Reagenzglas. Holt euch mit einem anderen Reagenzglas etwa 2 cm der Essigessenz (konzentrierter Essig), das ist unsere Säure. Gebt dann die Säure auf euren Stoff und beobachtet was passiert. Schwimmt der Stoff nur auf der Säure oder geht er unter? Oder bilden sich Bläschen, sobald die Säure mit eurem Stoff zusammenkommt. | {{Sicherheitsinfo|Schutzbrille}}'''Durchführung:''' Gebt etwa 0,5 cm eures Stoffes in ein sauberes Reagenzglas. Holt euch mit einem anderen Reagenzglas etwa 2 cm der Essigessenz (konzentrierter Essig), das ist unsere Säure. Gebt dann die Säure auf euren Stoff und beobachtet was passiert. Schwimmt der Stoff nur auf der Säure oder geht er unter? Oder bilden sich Bläschen, sobald die Säure mit eurem Stoff zusammenkommt. | ||
'''Entsorgung:''' Ins Waschbecken ausgießen und gut ausspülen. Eventuell mit einer Bürste Reste eures Stoffes entfernen. | '''Entsorgung:''' Ins Waschbecken ausgießen und gut ausspülen. Eventuell mit einer Bürste Reste eures Stoffes entfernen. | ||
| Zeile 226: | Zeile 226: | ||
{{ | {{Box|VERSUCH 6 - Sonstige Beobachtungen|Haltet alles fest, was euch sonst noch an dem Stoff auffällt. Denkt aber daran, dass ihr hier keine Spekulationen äußert, sondern möglichst neutral festhaltet, was wahrgenommen wird.}} | ||
| Zeile 232: | Zeile 232: | ||
{{Box|Stoffe identifizieren|2=Wir nutzen Stoffeigenschaften daher, um Stoffe zu identifizieren.|3=Hervorhebung}} | {{Box|Stoffe identifizieren|2=Wir nutzen Stoffeigenschaften daher, um Stoffe zu identifizieren.|3=Hervorhebung}} | ||
=== Fließschema zu Untersuchungen erstellen === | === Fließschema zu Untersuchungen erstellen === | ||
Version vom 23. Juli 2018, 20:05 Uhr
Chemie beschäftigt sich mit Stoffen. Was sind Stoffe aber genau?
Stoffe sind all die Materialien, aus denen unsere Welt zusammengesetzt ist. Wieviele Stoffe es genau gibt, kann man vermutlich nicht sagen, aber eine wichtige chemische Organisation gibt schon mal mindestens 30 Millionen als Anzahl an.
Am Anfang haben wir schon angesprochen, dass Chemie DIE Wissenschaft der Stoffe ist. Dabei spielen auch deren Eigenschaften eine große Rolle, denn Chemiher erfinden gezielt Stoffe mit bestimmten Eigenschaften wie man sie haben will. Oder Chemiker nutzen die Eigenschaften, um Stoffe zu indentifizieren.
Der Begriff "Stoff" ist vermutlich für dich noch etwas abstrakt und daher werden wir uns dem Begriff erst einmal nähern, indem wir bestimmte Stoffe betrachten, mit denen wir im Chemie-Labor öfters arbeiten werden.
Die Materialien der Laborgeräte
Warum verwendet man eigentlich für einige Tätigkeiten im Labor bestimmte Geräte nicht? Man könnte einfach sagen, weil sie dafür auch nicht gemacht sind. So sind die Maßangaben auf den Bechergläsern und Erlenmeyerkolben nicht genau genug sondern eher dafür da, eine grobe Einschätzung vornehmen zu können. Manchmal kommt es eben nur darauf an, ob man so ungefähr 100 ml Wasser. Ob es aber etwas mehr oder weniger sind, ist für den normalen Einsatz der Bechergläser nicht wichtig.
Ein anderer Aspekt bei der Auswahl der Geräte ist das Material, aus dem sie bestehen. Hier sind verschiedene Arten von Stoffen im Einsatz, die mit ihren Eigenschaften wichtig für eine sinnvolle Benutzbarkeit sind. Holz ist nun mal brennbar und Glas nicht wirklich biegsam und stabil.
Nachdem du die Geräte kennengelernt hast kannst du sie dir noch einmal anschauen unter dem Aspekt des Materials, aus dem sie bestehen. Warum das wichtig ist, wird in der nächsten Aktivität behandelt.
Nicht nur der Name ist wichtig, du musst auch wissen, für was du ein Gerät verwenden kannst und für was nicht. Dabei spielt das Material die wichtigste Rolle!
Wikipedia ist kein Kinder- und Jugend-Lexikon! Dennoch kann man auch schwierige Artikel verstehen. Wie man da am besten vorgeht wird hier behandelt und geübt:
Okay, mit den Materialien, aus denen die Laborgeräte bestehen, solltest du dich nun auskennen - merke dir die wichtigen Eigenschaften um die Geräte und dich zu schonen. Will man, was die Stoffe betrifft, etwas genauer sein, so kann man aber nicht alle Materialien als chemischen Stoff bezeichnen. Und zwar ist das Holz - ein natürliches Material - eben kein reiner Stoff sondern ein Gemisch, dass zum Beispiel auch Wasser enthält und das Lignin. Und je nachdem, welche Sorte Holz man hat, sind dessen Eigenschaften dank verschiedener Anteile und Beimischungen recht unterschiedlich. Das ist für Chemiker zu ungenau. Und das gilt für alle Naturstoffe, weswegen man diese meist in der Chemie nicht als Beispiele nimmt.
Nun aber mal wirklich genauer: was sind chemische Stoffe?
Stoffe im chemischen Sinne
Ein chemischer Stoff ist ein Material oder allgemein alles in den Naturwissenschaften, was man man beobachten und untersuchen kann und auch eine Masse besitzt. Raumbereiche, die keine Materie enthalten, bezeichnet man als Vakuum. Elektromagnetische Wellen, wie zum Beispiel Licht werden ebenfalls nicht zur Materie gezählt. Umgangssprachlich werden chemische Stoffe auch mit dem Wort Substanz bezeichnet, das im Sprachgebrauch der Chemie aber auf Stoffe in fester Form, sogenannte Feststoffe, beschränkt ist. Sonst hat man Flüssigkeiten oder Gase.
Stoffe in der Chemie werden grob unterschieden in Reinstoffe (Elemente oder Verbindungen) und Gemische. Es gibt weitere Unterteilungen, zu denen wir dann später noch kommen werden.
Wichtige Reinstoffe in der Chemie, die du schon kennen wirst, sind z. B. Wasser, Kochsalz (Natriumchlorid), Eisen, Alkohol (Ethanol)
Wichtige Stoffgemische sind zum Beispiel Luft, Salzsäure, Natronlauge (wie auf den Laugenbrezeln), Bronze, uvm.
Jede Stoffportion besitzt eine Masse, hat ein Volumen (also einen Platzbedarf) und besitzt eine innere Energie bzw. Wärmeenergie. Die Form eines Körpers kann auch bei gleichem Stoff (Material) unterschiedlich sein (z. B. Eisendraht, -pulver, -blech, -kugeln, -wolle).
- Ein Stoff (genauer Reinstoff) ist etwas, das eine Masse besitzt und dessen Eigenschaften man untersuchen und genau bestimmen kann.
- Gemische enthalten verschiedene Stoffe und deshalb hängen die Stoffeigenschaften davon ab, wieviel von den einzelnen Bestandteilen enthalten sind. Allerdings kann man es nicht immer erkennen, ob ein Stoff rein oder ein Gemisch ist.
- Gegenstände haben Eigenschaften, die von ihrer Form abhängen.
- Stoffklassen sind Gruppen von Stoffen, die ähnliche Eigenschaften haben.
- Erst mal eine einfache Übung: Gemisch oder Reinstoff?
- Ordne in der folgenden Aufgabe Stoffe, Gemische, Gegenstände und Stoffklassen zu. Start der Übung
Stoffeigenschaften
Eine Stoffeigenschaft ist eine, für einen bestimmten Stoff, typische Eigenschaft. Sie kann mit den Sinnen wahrgenommen werden (z. B. der Geruch) oder nur mit Messgeräten erfassbar sein.
In der Chemie unterscheidet man Reinstoffe von Stoffgemischen, denn Reinstoffe haben immer die gleichen Eigenschaften, während bei Stoffgemischen die Eigenschaften von den Mischungsverhältnissen der Komponenten abhängen.
Wie du schon bei den Laborgeräten feststellen konntest, sind die Stoffeigenschaften wichtig für deren Anwendung. Wir werden aber bald noch eine wichtige Bedeutung kennenlernen.
Sammelt in Gruppen - in die ihr im Unterricht eingeteilt werdet - gemeinsam Stoffeigenschaften. Öffnet dann bitte nur den einen Link, der zu eurer Gruppe gehört.
WICHTIG: Löscht nicht die Einträge von anderen Schülern (höchstens Rechtschreibefehler korrigieren)! Wenn ihr einige zusammen habt, sortiert die Eigenschaften.
So könnte man sortieren:
- Physikalische Stoffeigenschaften ... die man meist durch Messgeräte bestimmen kann.
- Chemische Stoffeigenschaften ... wo es um das Verhalten des Stoffes in chemischen Reaktionen geht.
- Physiologische Eigenschaften ... Stoffeigenschaften bei denen es um Wahrnehmbarkeit oder die Auswirkungen auf die Umgebung geht.
Eine Stoffeigenschaft ist eine für einen bestimmten Reinstoff typische Eigenschaft. Sie kann mit den Sinnen wahrgenommen werden oder nur mit Messgeräten erfassbar sein.
Eine Stoffeigenschaft hängt nicht ab ...
- von der Form (spitz, gebogen)
- von der Menge (schwer, leicht, groß, klein)
- von persönlichem Befinden oder Vorlieben (schwer herzustellen, schön, ...)
- von der Art der Gewinnung (nachwachsender Rohstoff, schwer herzustellen, ...)
- von den Bedingungen der Umgebung, wie zum Beispiel der Temperatur (fest, weich, hart, ...)
Wenn man die von euch genannten Eigenschaften etwas sortiert und fachlicher formuliert, dann haben wir das da bisher:
| Physikalische Stoffeigenschaften | Chemische Eigenschaften | Physiologische Eigenschaften |
|---|---|---|
|
Werte, welche durch Messung und Experimente bestimmt werden. |
Verhalten in chemischen Reaktionen. |
Wahrnehmungen oder Auswirkungen auf die Umgebung |
|
|
|
- Halte das rote Kästchen im Heft mit der Überschrift "Stoffeigenschaften" fest.
- Bearbeite das Zuordnungs-Quiz mit den Stoffeigenschaften und halte die weiteren Eigenschaften daraus mit der Tabelle oben fest.
- TIPP: Der Artikel Liste von Stoffeigenschaften liefert ein paar kurze Informationen zu den Stoffeigenschaften.
Nutzung der Stoffeigenschaften zur identifizierung eines unbekannte Stoffes
Wie du schon gelernt hast, nutzen Chemiker Stoff-Eigenschaften, um unbekannte Stoffe zu identifizieren. Das sollst du in deiner Gruppe nun auch gleich machen. Hoffentlich erinnerst du dich noch an die Namen der Geräte und wie man damit umgeht, denn nun wird es ernst!
Gegeben ist ein unbekannter weißer Feststoff, der pulverförmig ist. Es kommen fünf verschiedene Stoffe in Frage, die wir kennen. Das sind:
- Vitamin C
- Natron
- Backpulver
- Zucker
- Salz
Experimente zur Untersuchung des (noch) unbekannten, weißen Feststoffes
An Materialien wird benötigt:
- Einige saubere Reagenzgläser
- 1 schmutziges Reagenzglas
- Reagenzglasständer, Reagenzglashalter
- Gummistopfen, Spatel
Die folgenden Experimente sollen durchgeführt werden, wobei jede Gruppe nur einen Stoff untersucht. Teilweise findest du bei den Experimenten vertiefende Informationen zu einzelnen Eigenschaften, die du vielleicht noch nicht so kennst.
- Anschließend an dieses Experiment kann das Experiment Nr. 3 durchgeführt werden!
Durchführung: Füllt das Reagenzglas halbvoll mit Wasser. Gebt eine kleinere Menge (etwa 0,5 cm auf dem Spatel) eures Stoffes in das Wasser und schüttelt unter Verwendung des Gummistopfens. Überprüft, ob sich alles gelöst hat, oder ob noch Bodensatz vorhanden ist. Beobachtung: Nutzt die Begriffe löslich, unlöslich, Bodensatz zusammen mit Mengenangaben (wieviel Spatelspitzen), um die Löslichkeit zu beschreiben.
Generell gilt: Ein Stoff kann immer nur in einem Lösungsmittel löslich. Neben Wasser kann man auch die Löslichkeit in Benzin testen. Einige Stoffe, die nicht in Wasser löslich sind, kann an dagegen mit Benzin lösen. Es sind aber auch andere Kombinationen möglich.
- Man bezeichnet einen Stoff zum Beispiel "in Wasser löslich", wenn man eine bestimmte Menge eines Feststoffs in Wasser geben kann und er ist dann nicht mehr zu sehen.
- Als "Bodensatz" bezeichnet man Feststoff, der in das Wasser gegeben wurde, sich aber nicht auflöst und dann meist mit der Zeit absinkt. Er hat sich dann am Boden abgesetzt. Es kann sein, dass sich ein Teil des im Wasser gegebenen Feststoffes im Wasser löst und ein anderer sozusagen Teil als Bodensatz übrig bleibt. Dies kann man testen, indem man die Lösung verdünnt, also Wasser hinzugibt.
- Man bezeichnet einen Stoff "unlöslich", wenn selbst kleinste Menge in viel Lösungsmittel komplett als Bodensatz zurückbleiben. Bildet sich zum Beispiel erst nach der zweiten Spatelspitze Bodensatz, hat sich aber beim ersten Mal alles gelöst, so ist der Stoff nicht unlöslich. Er ist dann eher schwer löslich. Daher darf man am Afnang nicht gleich zuviel von dem Stoff ins Wasser geben.
- Das Experiment sollte immer nach dem Experiment Nr. 2 durchgeführt werden! Führt deshalb erst Nr. 2 durch und dann Nr. 3. Bringt also diese Anleitung erst noch einmal zurück, wenn ihr Nr. 2 noch nicht durchgeführt habt.
Durchführung: Holt euch ein weiteres sauberes Reagenzglas, gebt soviel destilliertes Wasser wie im anderen Reagenzglas aus Experiment Nr. 2 hinein. Stellt die beiden Reagenzgläser nebeneinander in den Reagenzglasständer. Gebt nun vom sogenannte Universalindiktor in die Reagenzgläser, und zwar in beide gleich viele Tropfen. Die Farbe des Wasser dient als Vergleichslösung, um die Färbung der Lösung beurteilen zu können. Ist die Farbe der Lösung ...
- wie beim Wasser, ist die Lösung neutral.
- rötlich, so ist die Lösung sauer.
- bläulich, so ist die Lösung alkalisch
Der pH-Wert ist ein Zahl, mit der eine bestimmte Eigenschaften einer Lösung beschrieben wird.
- Wasser hat den pH-Wert 7 und wird als neutral bezeichnet.
- Eine saure Lösung hat einen pH-Wert von 0 bis 7, wobei 0 sehr sauer ist und z.B. 6 nur ein wenig sauer ist. Sauer ist hier gleichbedeutend mit "schmeckt sauer".
- Eine alkalische Lösung (Lauge) hat einen pH-Wert von 7 bis 14, wobei 8 ein wenig alkalisch und 14 sehr alkalisch ist. Alkalische Lösungen lassen sich auch am Geschmack erkennen, aber es schmeckt wie Seife. Bekannt sind Seifenlauge und Laugenbrezel.
Entsorgung: In den Abfluss gießen, Reagenzgläser und Waschbecken gut mit Wasser ausspülen.
Durchführung: Gebt ganz wenige Körnchen eures Stoffes auf eines der gelben Scheiben und stellt dann die Mikroskop-Kamera darüber eventuell kann man an dem großen, silbernen Drehrad an der Kamera das Bild etwas schärfer stellen. Beschreibt, was ihr seht:
- Kann man an verschiedenen Körnchen immer wieder die gleiche Form erkennen und haben die Körnchen glatte Flächen, so hat man Kristalle.
- Ist die Oberfläche dagegen uneben und unregelmäßig, so sind das amorphe Körnchen.
Entsorgung: Kann weiter verwendet werden. Falls sich das Pulver über dem Tisch verteilt, bitte aufkehren und wegwerfen.
Kristalle sind Körper, die aufgrund einer regelmäßigen Anordnung der kleinsten Teilchen glatte Flächen aufweisen
Entsorgung: Ins Waschbecken ausgießen und gut ausspülen. Eventuell mit einer Bürste Reste eures Stoffes entfernen.
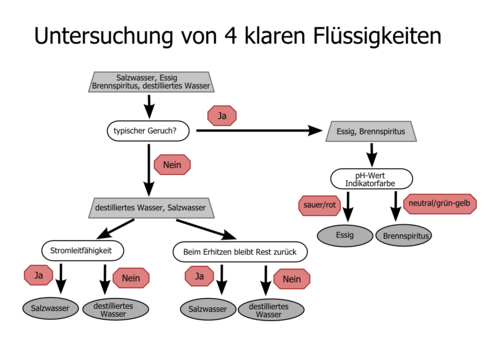
Fließschema zu Untersuchungen erstellen
Beispiel für 4 klare Flüssigkeiten
- Vorlage:Video Anleitungs-Video zur Benutzung der Vorlagen und des Programms Inkscape
- Vorlagen für das eigene Fließschema: Quer-Format und Hoch-Format