Benutzer:Cloehner/Salze/Vom Atom zum Ion: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung Markierung: 2017-Quelltext-Bearbeitung |
Keine Bearbeitungszusammenfassung Markierung: 2017-Quelltext-Bearbeitung |
||
| Zeile 4: | Zeile 4: | ||
=Die Reaktion von Aluminium mit Chlor= | =Die Reaktion von Aluminium mit Chlor= | ||
{{Aufgaben|1| | {{Aufgaben|1|Betrachtet das folgende Video zur Bildung von Aluminiumchlorid aus Aluminium und Chlor. Formuliert ein Versuchsprotokoll, in welchem ihr kurz und knapp die Durchführung, die Beobachtungen und die Auswertung in Form einer Reaktionsgleichung festhaltet.}} | ||
| Zeile 30: | Zeile 30: | ||
{{Aufgaben|2| | {{Aufgaben|2|Füllt die Lücken!}} | ||
<div class="lueckentext-quiz"> | <div class="lueckentext-quiz"> | ||
| Zeile 37: | Zeile 37: | ||
{{Aufgaben|3| | {{Aufgaben|3|Zieht die Karten auf den richtigen Platz. Übertragt den vollständigen Merktext in eure Unterlagen.}} | ||
<div class="lueckentext-quiz"> | <div class="lueckentext-quiz"> | ||
| Zeile 44: | Zeile 44: | ||
{{Aufgaben|4| | {{Aufgaben|4|Fertigt in euren Unterlagen unter dem Merktext ein Reaktionsschema mit den Schalenmodellen der beteiligten Atome und Ionen an, in dem die beschriebenen Veränderungen im Aufbau der Teilchen deutlich werden. | ||
{{Lösung versteckt|Die Animation zeigt, was während der Reaktion mit den Atomen passiert. Am Anfang des Videos seht ihr die Darstellung der Edukte, am Ende die der Produkte. | |||
[[Datei:Animation Ionenbildung.mp4|thumb|links]]}} | |||
}} | |||
==Zurück zum Aluminiumchlorid== | |||
Version vom 2. April 2019, 18:43 Uhr
Ihr habt die Halogene bereits als sehr reaktionsfreudige Elementfamilie kennengelernt. Mithilfe deines Wissens zum Bohr'schen Atommodell kannst du nun auch erklären, warum die Halogene so heftig reagieren.
Die Reaktion von Aluminium mit Chlor
Worin unterscheiden sich die Bestandteile des Aluminiumchlorids von den Atomen des Aluminiums und des Chlors?
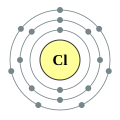
Offensichtlich bildet sich aus Aluminium und Chlor in einer exothermen Reaktion ein neuer Stoff, das Aluminiumchlorid. Aluminiumchlorid ist ein Salz, das völlig andere Eigenschaften aufweist als die Edukte Aluminium und Chlor. Die veränderten Eigenschaften des Produktes lassen dich durch Veränderungen im Aufbau der Aluminium- und Chloratome, die unten abgebiledet sind, erklären.
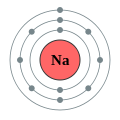
Vorüberlegung: Die Reaktion von Natrium mit Chlor.
Auch Natrium und Chlor reagieren in einer exothermen Reaktion zu Nariumchlorid, welches wir unter dem Namen „Kochsalz” kennen. Wir betrachten noch einmal ein Natrium- und ein Chlor-Atom im Vergleich:
Bei exothermen chemischen Reaktionen entstehen häufig aus reaktiven, instabilen Teilchen neue Teilchen, die weniger reaktiv und deshalb stabiler sind. Wie könnten die stabileren „Verwandten” der Natrium- und der Chloratome aussehen?
Die Elementfamilie des Periodensystems, deren Elemente deren Elemente die stabilstens, reaktionsträgsten Atome haben, ist die Familie der Edelgase(). Diese Stoffe stehen in der 8.|achten() Hauptgruppe des Periodensystems. Das besondere an den Atomen dieser Hauptgruppe ist, dass sie alle eine voll besetzte|volle() Außenschale haben.
Damit das Natrium-Atom die besonders stabile Elektronenverteilung eines Edelgases erreicht, muss es ein Elektron abgeben. Dies kann jedoch nur passieren, wenn es einen Reaktionspartner gibt, der das abgegebene Elektron aufnimmt. Bei der Bildung von Natriumchlorid übernehmen diese Rolle die Chlor-Atome. Auch für die Atome des Chlors ist diese Elektronenübertragung vorteilhaft, da auch diese durch die Aufnahme eines Elektrons mit acht Valenzelektronen eine voll besetzte Außenschale bekommen. Dadurch, dass sich die Anzahl der Elektronen verändert während die Anzahl der Protonen gleich bleibt, entstehen bei dieser Reaktion geladene Teilchen, die in der Chemie als Ionen bezeichnet werden.
Fertigt in euren Unterlagen unter dem Merktext ein Reaktionsschema mit den Schalenmodellen der beteiligten Atome und Ionen an, in dem die beschriebenen Veränderungen im Aufbau der Teilchen deutlich werden.