Chemie-Lexikon/Redoxreaktionen mit Elektronenübertragung
In der Mittelstufe werden die Begriffe Reduktion und Oxidation meist im Zusammenhang mit Verfahren zur Gewinnung von Metallen besprochen, wobei eine Übertragung von Sauerstoff stattfindet.
Wiederholung: Redoxreaktionen als Sauerstoffübertragungsreaktionen
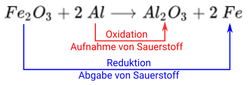
In der Mittelstufe kommen Redoxreaktionen im Rahmen der Verfahren zur Gewinnung von Metallen zur Sprache. Typischerweise betrachtet man die Reduktion von Kupfererzen mit Hilfe von Kohle und den Hochofen-Prozess. Aber auch bei der Thermitreaktion handelt es sich um ein Redoxreaktion:
Hier findet zum einen die Oxidation von Aluminium statt, hin zu . Zum anderen die Reduktion von hin zu Eisen.
Beide Teil-Reaktionen haben eine Funktion in der Gesamtreaktion.
- Die Oxidation von Aluminium liefert die für die Reduktion benötigte Energie, denn Oxidationen sind immer exotherm und Reduktionen endotherm. Aluminium ist daher auch das Reduktionsmittel.
- Die Reduktion von führt zur Freisetzung von Sauerstoff, was die Oxidation begünstigt und damit verstärkt. wirkt damit als Oxidationsmittel.
Noch ein kompakt die Begriffe zusammengefasst:
- Oxidation = Reaktion mit Aufnahme von Sauerstoff
- Reduktion = Reaktion mit Abgabe von Sauerstoff
- Oxidationsmittel = Stoff, der die Oxidation ermöglicht, indem er selber Reduziert wird.
- Reduktionsmittel = Stoff, der die Reduktion ermöglicht, indem er selber oxiddiert.
Redoxreaktionen ohne Sauerstoff
Betrachtet man Reaktionen an denen kein Sauerstoff beteiligt ist, dann kann man Gemeinsamkeiten zu den Reaktionen mit Sauerstoff erkennen.
Beispiel:
- 2 Cu + O_2 ⟶ 2 CuO
- Cu + S ⟶ CuS
In beiden Reaktionen geben die Kupferatome Elektronen ab und es entstehen Cu2
Das heißt, in beiden Beispiel reagiert das Kupfer genauso: es gibt sowohl bei der Reaktion mit Sauerstoff Elektronen ab, also auch bei der Reaktion von Kupfer mit Schwefel.
Geschichtliches und Verallgemeinerung
Der Begriff Oxidation wurde ursprünglich von dem französischen Chemiker Antoine Laurent de Lavoisier geprägt, der damit die Reaktionen von Elementen und chemischen Verbindungen mit dem Element Sauerstoff (Oxygenium, franz: oxygène) und dessen Aufnahme, unter Bildung von Oxiden, beschreiben wollte. Als Lavoisier die Theorie in den 1780er Jahren veröffentlichte, hatte er anfänglich gegen die Anhänger der Phlogiston-Theorie zu kämpfen, konnte sich aber durchsetzen.
Später erfolgte eine Erweiterung des Begriffes, indem man Reaktionen mit einbezog, bei denen einer Verbindung Wasserstoffatome entzogen wurden (Dehydrierung). Auf Grundlage der Ionentheorie und des Bohrschen Atommodells konnte die Oxidation schließlich unter Betrachtung der Aufnahme und Abgabe von Elektronen interpretiert und verallgemeinert werden.
Daher werden heute die Begriffe zu den Redoxreaktionen mit Hilfe der Aufnahem und Abgabe von Elektronen definiert.
- Oxidation = Elektronenabgabe
- Reduktion = Elektronenaufnahme
- Reduktionsmittel = Stoff, der beim Reaktionspartner die Reduktion bewirkt, indem er ihm Elektronen abgibt
- Oxidationsmittel = Stoff, der beim Reaktionspartner die Oxidation bewirkt, indem er ihm Elektronen abnimmt
- Oxidation = Sauerstoffaufnahme oder Elektronenabgabe
- Reduktion = Sauerstoffabgabe oder Elektronenaufnahme
- Reduktionsmittel = Stoff, der beim Reaktionspartner die Reduktion bewirkt, indem er ihm Elektronen abgibt
- Oxidationsmittel = Stoff, der beim Reaktionspartner die Oxidation bewirkt, indem er ihm Elektronen abnimmt




