Elementarteilchen und Radioaktiver Zerfall/Der Aufbau eines Atoms
Schon im antiken Griechenland haben sich Philosophen Gedanken zum Aufbau der Materie gemacht. Aus dieser Zeit stammt der Begriff des Atoms. Er leitet sich vom griechischen "atomos" ab, was übersetzt etwa so viel wie "nicht spaltbar" bedeutet. Die alten Griechen sind früher also davon ausgegangen, dass Materie aus kleinsten Teilchen mit dem Namen Atom bestehen und dass diese Atome der Materie ihre Eigenschaften geben.
Den Gedanken der "Nichtspaltbarkeit" kann man verstehen, wenn man sich z.B. einen Eisenwürfel vorstellt, den man halbiert. Dann stellt man sich vor, wie man die Hälfte des Eisenwürfels erneut halbiert. So macht man immer wieder weiter. Nach den Gedanken der alten Griechen ist dieses Verfahren nicht unendlich lang weiterführbar, weil man irgendwann nur noch das nicht spaltbare kleinste Eisenteil, das Eisenatom, übrig hat.
Etwa zwei Jahrtausende später entdeckt der Physiker J. J. Thomson die negativ geladenen Elektronen, die um ein Vielfaches kleiner sind als das Atom selbst. Außerdem gibt es Gründe zur Annahme, dass Elektronen Teil jedes Atoms sind. Das Bild der unteilbaren Atome ist erschüttert. Es stellt sich eine Frage: Wenn Atome insgesamt elektrisch neutral geladen sind, aber elektrisch negativ geladene Elektronen beinhalten, was für Teilchen existieren dann noch im Atom, um die negative Ladung auszugleichen?
Das motivierte viele Physiker und ein neues Forschungsgebiet entstand. Sie versuchten, ein Modell für den Aufbau der Atome zu erstellen. Ein erstes Modell kam von J. J. Thomson selbst. Er modellierte das Atom wie den Teig von Rosinenkuchen: Ein Atom sei laut Thomson ein Kügelchen gewesen, in dem Masse und positive Ladung gleichmäßig verteilt sind. In diesem Kügelchen eingebettet sind wie Rosinen im Kuchenteig die punktförmigen, negativ geladenen Elektronen.
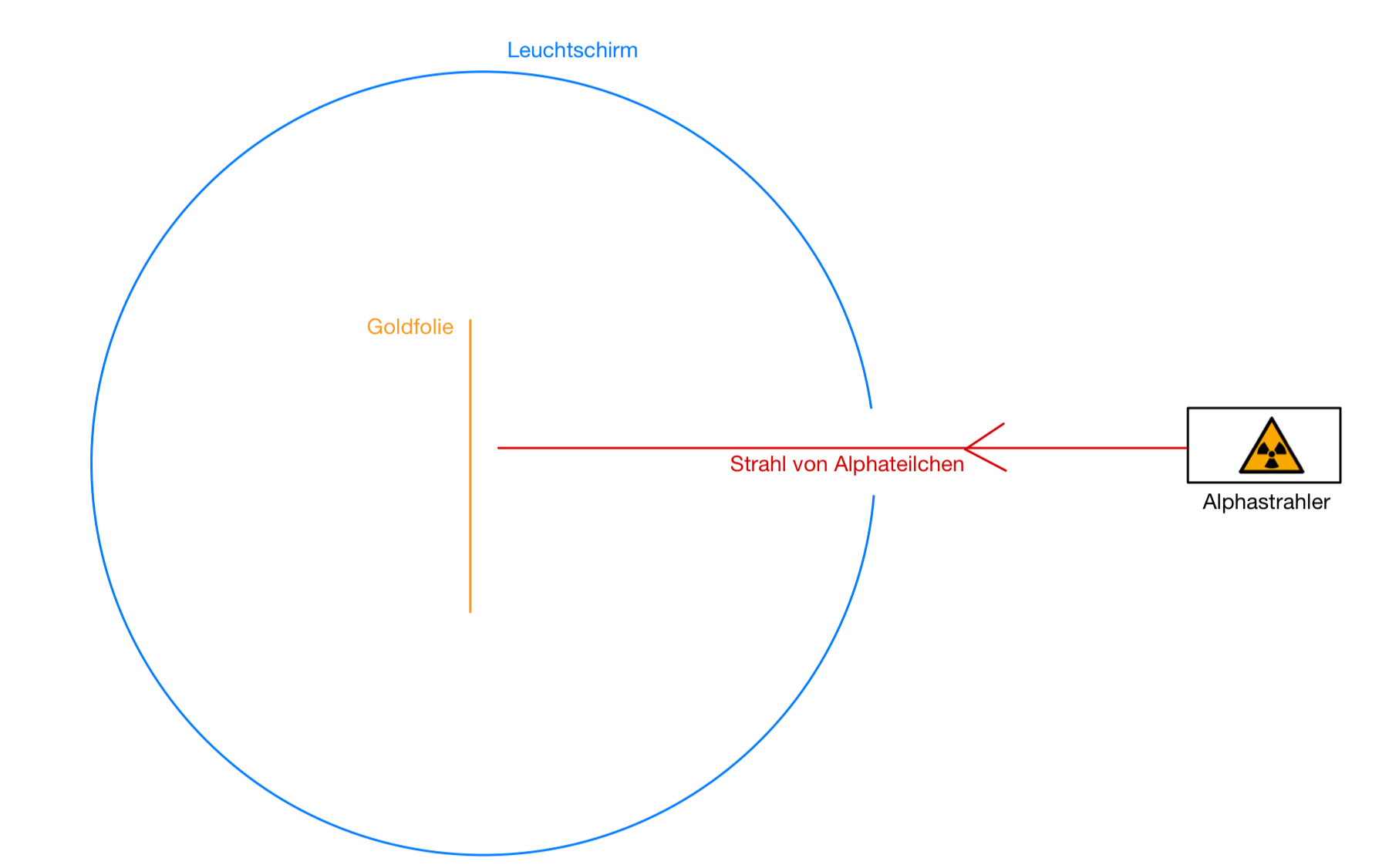
Der Physiker Ernest Rutherford wollte 1911 das Modell Thomsons überprüfen. Dazu führte er seinen Streuversuch durch. Er wird auf der Skizze dargestellt. In dem Versuch schoss er positiv geladene Alpha-Teilchen auf eine dünne Goldfolie.
Um die Goldfolie herum war ein Leuchtschirm. Er begann an den Stellen zu leuchten, wo er von Alpha-Teilchen getroffen wurde. So ließen sich Aussagen über die Bewegungsbahn der einzelnen Alpha-Teilchen treffen.
Simulation des Versuchs von Rutherford
Der Versuchsaufbau Rutherfords wird in der obigen Abbildung dargestellt. In der Simulation wird dargestellt, was bei dem Versuch auf atomarer Ebene passiert. Dabei wird im Rosinenkuchenatom gezeigt, wie der Versuch laufen würde, wenn Thomsons Modell stimmt und im Rutherfordatom, was tatsächlich beobachtet wurde. Führe den Versuch Rutherfords in der Simulation unter dem folgenden Link mit dem Rutherford-Atom durch.
Beschreibe deine Beobachtung beim Rutherford-Atom, indem du den Satzanfängen das passende Ende zuordnest
Die meisten Alpha-Teilchen bewegen sich unverändert weiter.
Ein paar Alpha-Teilchen werden leicht abgelenkt.
Wenige Alpha-Teilchen werden in ihre Herkunftsrichtung zurückgeworfen.
Erkläre, warum einige Alpha-Teilchen abgelenkt werden und andere nicht.
Deute, was das Verhalten der Alpha-Teilchen für den Aufbau des Atoms bedeutet.
Lerneinheiten
4. Nachweis von Radioaktivität
5. Verschiedene Arten von Strahlung
6. Aktivität