Das Teilchenmodell und die Schmelz- und Siedetemperatur
Das wir und die ganze Materie um uns herum nicht aus einem kontinuierlichen Material bestehen, wie es ganz früher in der Antike und teilweise auch von Kinder gesehen wird, sollte inzwischen jedem klar sein. Natürlich fällt einem sofort das "Atom" ein, denn alles um uns herum besteht aus Atomen. Wenn wir in der Chemie von Teilchen sprechen, sind aber nicht immer die Atome gemeint. Denn wenn wir alles aus Atomen besteht stellt sich die Frage, warum sich die Stoffe so verschieden verhalten.
Tatsächlich sind die "Teilchen" die wir in der Chemie betrachten verschiedene Teilchen, die zwar auch einzelne Atome sein können oder aber auch zusammengesetzte Teilchen wie Moleküle oder geladene Teilchen wie Ionen. In vielen Fällen reicht es aus, sich ein einfaches Teilchenmodell vorzustellen, wobei zunächst unwichtig ist, was für eine Art von Teilchen es genau ist.
Diese Seite stellt eine Zusammenfassung dar für Schüler der Oberstufe, die noch einmal alles wiederholen wollen. Es gibt keine große Herleitung sondern nur kurze und knappe Erklärungen. Dabei werden aber auch die typischen Probleme und Fehler angesprochen, die öfters gemacht werden.
Das einfache Teilchenmodell
Für dieses einfache Teilchenmodell gelten folgende Regeln:
- Alle Stoffe bestehen aus kleinsten Teilchen und zwischen den Teilchen ist leerer Raum.
- Die Teilchen verschiedener Stoffe unterscheiden sich in Größe und Masse.
- Alle Teilchen sind ständig in Bewegung. Je höher die Temperatur, desto schneller bewegen sich die Teilchen.
- Zwischen den Teilchen gibt es Anziehungskräfte, die bei verschiedenen Stoffen unterschiedlich stark ist.
Wenn man diese Eigenschaften betrachtet, so sollte man sich klar machen, dass wir hier quasi Reinstoffe betrachten. Der Reinstoff Sauerstoff enthält eben nur eine Sorte von Teilchen (hier ein zweiatomiges Molekül). Andere Teilchen gibt es in dem Reinstoff nicht und dementsprechend gibt es zwischen den Sauerstoffteilchen keine andere Teilchen. Ist Sauerstoff aber Bestandteil der Luft, einem Gemisch, so habe ich natürlich nicht nur die Teilchen vom Sauerstoff sondern auch die Teilchen vom Stickstoff, von den Edelgasen, vom Kohlendioxid usw. und eventuell von Verunreinigungen. Alles sind Teilchen, es gibt nichts anderes!
Häufig auftretende Fehler beim Teilchenmodell:
- Die Eigenschaften eines Stoffes ergeben sich erst aus der Anhäufung von mehreren Teilchen. Die Anziehung der Teilchen untereinander ist natürlich auch bei zwei Teilchen vorhanden.
- Ein kleinstes Teilchen hat keine Farbe. Die Farbe in den Elektronenmikroskop-Aufnahmen sind vom Computer erzeugt! Ein Farbeindruck entsteht dadurch, das ein Teil des weißen Licht durch den Gegenstand, den wir betrachten, verschluckt wird (Absorption). Das sichtbare Restlicht ergibt den Farbeindruck eines Gegenstandes (siehe Remission
 ). Und einzelne Teilchen können kein Licht zurückwerfen, da sie zu klein sind.
). Und einzelne Teilchen können kein Licht zurückwerfen, da sie zu klein sind.
Nun gehen wir die Informationen zum Teilchenmodell kurz noch einmal durch. Dazu zwei Videos, mit Erklärungen dazu.
Schau dir den Film einmal an, bevor du den Text danach weiterliest!
Vergleich der Teilchen
In jedem der Kästchen siehst du zwei Teilchen. Sie sollen verschieden sein, was durch die Farbe und einen Größen-Unterschied verdeutlicht wird. Wir werden uns bald noch mehr solcher Simulationen anschauen und daher muss klar sein, das die Farbe und die Größe nur dafür da sind um zu verdeutlichen, dass es nicht die gleichen Teilchen sind. Anhand der Größe könnte man natürlich auf die Masse schließen, was aber nicht erwünscht ist. Ebenso sind die Farben willkürlich gewählt, sind haben nichts nicht der Eigenschaften zu tun. Ebenso so verzichten wir darauf, die Form der Teilchen anderes dazustellen, obwohl du sicher weißt, dass es große und kleine Moleküle gibt. Wichtig ist nur: "Andere Teilchen gehören zu anderen Stoffen".
Der Aspekte der Anziehung der Teilchen
Die Anziehung ist unsichtbar, aber man kann bei den drei verschiedenen Teilchentypen, die ich da in der Simulation dargestellt habe, deutliche Unterschiede erkennen. Je stärker die Anziehung ist, desto mehr bleiben die Teilchen zusammen. Dabei ist die Anziehung aber nicht so wie bei einem Magneten: kommt ein Stück Eisen in die Nähe von einem Magneten wird es angezogen und hängt dann da fest. Aber wir haben ja die Grundregel, dass die Teilchen immer in Bewegung ist, auch wenn sie sich gegenseitig anziehen. Und so kann es vorkommen, dass sich die Teilchen mal wieder trennen.
Dieser Text bezieht sich auf das nächste Video. Lies erst einmal diesen Text durch, bevor du das Video anschaust!
Zusammenhang Temperatur und Teilchenbewegung
Wie schon erwähnt, sind die Teilchen immer in Bewegung. Der Film zeigt nur ein einzelnes Teilchen. Im Grund genommen gibt es das nicht, aber so verlieren wir nicht den Überblick. Wichtig zu wissen ist, dass die Temperatur zunächst keine Auswirkung auf das Teilchen hat, weil die Wärme (eine Energie-Art) nicht so einfach verloren geht. Erst die Interaktion mit den Wand führt zu einer veränderten Geschwindigkeit des Teilchen. Die Wände geben die Wärme/Energie an das Teilchen weiter oder nehmen Wärme/Energie vom Teilchen weg. Eigentlich müssten die Wände ja auch aus Teilchen bestehen, aber das missachten wir hier und sehen sie als eine Blackbox an, die die Fähigkeiten hat, die ich eben beschrieben habe.
Okay, eigentlich ist das ja nichts Besonderes: je wärmer desto schneller ist ein Teilchen. Es ist nicht immer gleich schnell, denn die Aufnahme von der Wand bzw. die Abgabe an die Wand ist ein zufälliger Vorgang. In einer späteren Simulation mit mehreren Teilchen kommt das dadurch zustande, das ich viele Teilchen habe und die sich verschiedenen gegenseitig anstoßen oder abbremsen.
Schon mit dieser einfachen Überlegung kann man viele Dinge erklären.
- Wenn die Teilchen sich beim Abkühlen immer langsamer bewegen gibt es natürlich eine Temperatur, bei der sich die Teilchen nicht mehr bewegen. Kälter kann es dann nicht werden, da die Teilchen nicht langsamer sein können, als still zu stehen. Das wäre beim absoluten Nullpunkt bei etwa -273°C = 0K (Kelvin).
- Wenn wir einen warmen Gegenstand anfassen, spüren wir an unserer Hand die Reibung der Teilchen. Je schneller die sich bewegen, desto mehr reiben sie an unserer Hand und diesen Unterschied können wir spüren, wenn wir unterschiedliche Temperaturen haben.
- Wir können so auch die Übertragung von Wärme erklären, denn warmes Wasser kann seine Wärme an das Metall abgeben, indem die schnellen Wasserteilchen an die Metallteilchen anstoßen und sie so zu einer schnelleren Bewegung bringen, was eine höhere Temperatur beim Metall bedeutet.
Und so weiter ...
Auf diese Art und Weise kann man weitere Phänomene rund um Wärme erklären. In diesem Fall ist es wichtig, das die von uns "von außen" zu messende Wärme (wird vom Thermometer angezeigt!) mit Hilfe der Teilchen (dem "Inneren" des Stoffes) erklärt werden kann. Solche Argumentationen werden gerne abgefragt, denn sie zeigen, wie gut ein Schüler diesen Zusammenhang verstanden hat.
Was hier auch deutlich sein sollte: wir haben jetzt gerade nicht die Art der Teilchen betrachtet. Die Möglichkeit, dass große Moleküle sich in sich natürlich auch bewegen können (biegen, verdrehen) usw. stört hier nur und wird daher ignoriert.
Die Aggregatzustände und das Teilchenmodell
Ganz wichtig: Aggregatzustände können wir nur haben, wenn wir eine größere Menge an Teilchen haben.
Vorab erst einmal ein Hinweis auf typische Fehler: Öfters bekommt man solche Formulierungen zu hören, wie "Das Teilchen ist flüssig" oder "gasförmige Teilchen". Das ist aber falsch, denn Teilchen in einer Flüssigkeit unterscheiden sich nicht von den Teilchen des gleichen Stoffes im festen Zustand. Was der Unterschied ist, werden wir uns gleich anschauen. Unter andren sind die Teilchen aber bei dem flüssigen Stoff schneller in Bewegung, denn um einen festen Stoff flüssig zu bekommen muss man ihn erwärmen.
Nun wieder zu einer Simulation. Wir beobachten hier viele Teilchen auf einmal. Die Änderung der Temperatur hat eine Änderung der Geschwindigkeit bei jedem einzelnen Teilchen zur Folge, wie auf ein einzelnes Teilchen, dass alleine ist. Allerdings kann man, je nach Anziehung der Teilchen und der Geschwindigkeit beachten, dass das Bild nicht immer das gleiche ist.
Hinweis: Das die Teilchen nach unten fallen, bzw. sich eher weiter unten aufhalten hat damit zu tun, dass eine Schwerkraft simuliert wird. Wenn die ausgeschaltet wäre, würden auch langsame oder zusammenhängende Teilchen nicht "unten" liegen sondern herumschweben. Die Position der Teilchen hat also eher einen geringere Bedeutung.
Was zu beobachten ist:
Neben der Veränderung der Temperatur am Schieberegler kann man sich die Bewegung von einem einzelnen Teilchen anschauen: Bewegt es sich schnell/langsam? Bewegt es unabhängig von den anderen Teilchen oder stößt es öfters an andere Teilchen an?
Außerdem sollte man die Gesamtheit der Teilchen betrachten: Sind die Teilchen eng beeinander oder ist viel Platz zwischen ihnen? Wieviel Platz nehmen sie ingesamt ein? Sind sie geordnet oder ungeordnet?
Es fällt auf, dass es beim Aussehen der Teilchen deutliche Unterschiede gibt. Man kann im Grunde genommen drei verschiedene Arten der Anordnungen der Teilchen festhalten.
Diese drei Zustände/Anordnungen kann man als Aggregatzustände des Stoffes (von dem wir hier die Teilchen haben) ansehen. Sie hängen von der Temperatur ab.
Exkurs: Aggregatzustände
Das ist Grundwissen, das man parat haben muss.
- Die Begriffe fest, flüssig und gasförmig ist die formalen Bezeichnungen der drei Aggregatzustände. Man muss aufpassen, dass man hier und auch bei den Übergängen zwischen den Aggregatzuständen diese Namen, nicht mit speziellen Bezeichnungen für das Wasser, verwechselt, was gerne als Beispiel verwendet wird. Also: Eis ist Wasser im festen Zustand!
- Im folgenden Bild wird auch wieder Wasser betrachtet und anhand der drei Aggregatzustände werden die Bezeichnungen für die Übergänge aufgeführt. Spezielle beim Wasser gibt es einige Bezeichnungen, die sehr gebräuchlich sind.

Typische Fehler:
Wolken oder Wasserdampf werden gerne als gasförmig bezeichnet. Korrekterweise müsste man das als falsch ansehen, denn gasförmige Wasser ist unsichtbar! Das kennen Sauna-Besucher, denn der Aufguss verschwindet meist ins Nichts!
Was man bei Wolken oder Dampf sieht sind Wassertröpfchen mit mehreren Teilchen. Diese Ansammlung an Teilchen ist groß genug, damit sie sichtbar sind. Gasförmiges Wasser wäre genauer gesagt Luftfeuchtigkeit.
Für die Übergänge sind zwei Werte wichtig, der Schmelz- und die Siedetemperatur oder auch Schmelz- und die Siedepunkt.
Die Definitionen sollten klar sein:
- Die Schmelztemperatur ist die Temperatur bei der ein Stoff schmilzt, also ein fester Stoff beim Erhitzen flüssig wird. Umgekehrt ist das aber auch die Temperatur, bei der flüssiger Stoff fest wird, wenn man ihn abkühlt.
- Gleiches bei der Siedetemperatur: es ist die Temperatur bei der einer flüssiger Stoff gasförmig wird, wenn man ihn erwärmt oder umgekehrt die Temperatur bei der ein gasförmiger Stoff flüssig wird wenn man ihn abkühlt.
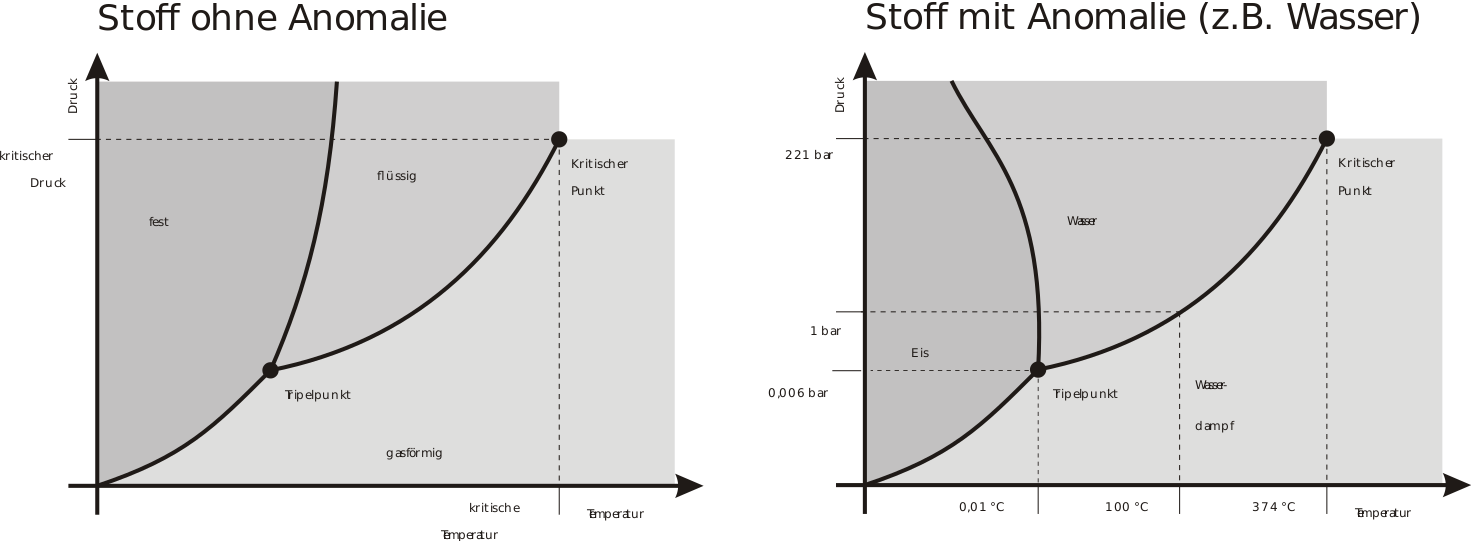
Die Diskussion um "-punkt" oder "-temperatur" lässt sich verschieden begründen. "Temperatur" scheint sinnvoller, aber die Befürworter von "Punkt" sehen solche Phasendiagramme, wie die zwei Folgenden. Denn die Temperaturen sind vom Druck abhängig und so kann man in solchen Diagrammen sehen, welcher Aggregatzustand der Stoff (dessen Phasendiagramm man vor sich hat) bei einem bestimmten Druck und einer bestimmten Temperatur hat.
Beim Phasendiagramm von Wasser ist zum Beispiel bei der y-Achse 1 bar eingetragen und man kann da, wo die gestrichelte Linie bei 1 bar die Trennlinien zwischen den Aggregatzuständen schneidet, die entsprechenden Temperaturen ablesen. Das wäre beim Wasser (siehe x-Achse) bei 0,01 °C bzw. 100°C.
Die Eigenschaften der Aggregatzustände mit dem Teilchenmodell erklären
- Kommt noch -
Woher kommen die verschiedenen Siedetemperaturen?
In dem einen Video vorhin haben wir gesehen, dass Teilchen sich unterschiedlich stark anziehen können. Wenn man drei verschiedene Teilchen mit unterschiedlicher starker Anziehung hat, kommt man zu drei Stoffen, die verschiedene Schmelz- und Siedetemperaturen haben.
Das folgende Video zeigt drei solche verschiedenen Stoffe. Die Teilchen wurden verschieden eingefärbt, um zu verdeutlichen, dass sie nicht identisch sind. Man erkennt deutlich, dass zu Beginn des Films die drei Stoffe in verschiedenen Aggregatzuständen vorliegen:
- Der Stoff links ist bei der Anfangstemperatur ein Feststoff.
- Der mittlere Stoff ist eine Flüssigkeit.
- Der Stoff rechts ist gasförmig.
Folgendes ist im Laufe des Films noch zu beobachten:
- Beim Erhöhen der Temperatur geht der mittlere Stoff schnell in den gasförmigen Zustand über.
- Der linke Stoff allerdings ist erst bei der höchsten Temperatur dabei zu schmelzen. Die Teilchen sind nicht mehr alle an einer festen Position. Dieser Stoff hat also eine sehr hohe Schmelz- und Siedetemperatur.
- Durch das Absenken der Temperatur wird die Geschwindigkeit aller Teilchen geringer. Bald bleiben die Teilchen des mittleren Stoffes auf ihrer Position und bewegen sich nur noch auf ihren Platz. Der Stoff ist erstarrt.
- Erst bei ganz niedrigen Temperaturen ist die Geschwindigkeit der Teilchen des rechten Stoffes klein genug, damit die sehr schwachen Anziehungskräfte wirken können. Allerdings reicht die niedrige Temperatur nur dafür aus, um den Stoff zu verflüssigen. Dieser Stoff hat eine sehr niedrige Siedetemperatur, denn schon bei der geringsten Erwärmung wird der Stoff wieder gasförmig.
Welche Arten von Teilchen und Anziehungen gibt es?
Mal vorab etwas SEHR wichtiges:
Daher schauen wir uns nun einmal alle Typen von Teilchen an und klären, wie ich erkennen kann, ob ein Stoff/eine Verbindung Teilchen von einem bestimmten Typ hat.
Was sich auf die Schmelz- und Siedetemperatur auswirkt
Nach der Stärke sortiert sind es die folgenden Eigenschaften, die sich auf die Schmelz- und Siedetemperatur auswirken
- Masse
- Van-der-Vaals-Kräfte
- Polarität/Dipol
- Wasserstoff-Brücken-Bindung
- Ionenbindungen
Natürlich kann es sein, das mehrere dieser Eigenschaften zusammenkommen. Wenn man zum Beispiel die gleiche polare Gruppe in zwei Molekülen hat, dann spielt eventuell auch die Masse eine Rolle.
Was diese Eigenschaften bedeuten, wie sie zustande kommen und woran ich erkenne, ob ein Stoff Teilchen mit diesen Eigenschaften hat, wird bei den einzelnen Teilchenarten genauer angesprochen.
Teilchenarten
Atome
Die einfachsten, kleinsten Teilchen sind die Atome. Sie kommen normalerweise nur vor in Elementen einzeln vor, allerdings gibt es einige Elemente, die nicht einzelne Atome sondern Moleküle enthalten, wie die gasförmigen Elemente Wasserstoff H2, Sauerstoff O2, Stickstoff N2, die Halogene F2, Cl2, Br2, I2.
Einzelne Atome enthalten üblicherweise:
- von den Nichtmetallen nur die Edelgase, also Helium, Neon, Argon, Krypton, Xenon und Radon
- die Metalle allgemein könnte man dazu zählen, allerdings könnten wir sie auch als Riesenmoleküle bezeichnen, was gleich noch genauer angesprochen wird.
Die Atome bei den Edelgasen kann man eigentlich direkt mit einfachen Kugeln in der Simulation vergleichen. Einzelne Atome haben keinen Grund sich anzuziehen. Obwohl wir natürlich positive und negative Ladungen im Atom selber haben, so ist das Atom nach außen hin neutral und damit gibt es auch keine Anziehung. In kleinem Maß können da die Van-der-Waals Kräfte eine Rolle spielen, bei denen darum geht, dass durch die Bewegung der Elektronen in der Hülle es zufällig passieren kann, dass an einer Stelle mehr Elektronen sind. Das wird später erklärt und man muss auch bedenken, dass die Van-der-Waals Kräfte sehr schwach sind. Wichtiger ist aber ein anderer Aspekt. Vorher schauen wir uns kurz die Daten an:
| Element | Helium | Neon | Argon | Krypton | Xenon | Radon |
|---|---|---|---|---|---|---|
| Schmelztemperatur | -272,2 °C | -248,6 °C | -189,3 °C | -157 °C | -112 °C | -71 °C |
| Siedetemperatur | -268,9 °C | -245,9 °C | -185,8 °C | -152,9 °C | -107,1 °C | -61,8 °C |
| Atommasse [u] | 4 | 20,2 | 38,9 | 83,8 | 131,3 | 222 |
Im Grunde genommen reicht, es eine der Zeilen zu betrachten, wie zum Beispiel die Siedetemperatur. Man sieht das die Siedetemperatur von Helium bis zum Radon zunimmt, denn -268°C ist ja weniger als -61°C. In der Zeile untendrunter stehen noch die Atommassen und die sind der wesentliche Grund, warum sich die Siedetemperatur erhöht.
Je schwerer die Atome (und auch allgemein die Teilchen) sind desto schwieriger sind sie in Bewegung zu bringen. Bei Erhitzen bewegen sich die Atome/Teilchen ja immer schneller, aber schwerere Teilchen sind schlechter in Bewegung zu bringen als kleine und leichte. Man vergleiche vielleicht kleine Murmeln (~ 4 g), die ich in einem Behälter habe. Mir fällt es recht leicht, das Gefäß zu schütteln und damit die Kugeln im Gefäß rumfliegen zu lassen. Schwere Kugeln (vielleicht eine Grapefruit mit ~ 220 g ≈ knapp eine Butterpackung) würden viel mehr Kraft und damit Energie erfordern. Gerade beim Sieden bewegen sich die Atome ja nicht nur um sich herum in der Flüssigkeit sondern bewegen sich unabhängig voneinander im Raum, auch nach oben. Bei schweren Teilchen ist das wesentlich schwieriger.
MERKE Je schwerer ein Teilchen in einem Stoff ist, desto schwerer sind die Teilchen beim Erhitzen in Bewegung zu bringen.
- Deshalb erfordert es mehr Energie bis die Teilchen sich schnell genug bewegen, um sich von einander zu trennen, was zum Beispiel für das Sieden zu notwendig ist.
Polare und Unpolare Moleküle
Moleküle sind ja zusammengesetzte Teilchen, die aus mehreren Atomen bestehen, die dauerhaft zusammenhalten. Die Atome sind über sogenannte Atombindungen/Elektronenpaarbindungen stabil miteinander verbunden. Wir gehen davon aus, das die Moleküle stabil sind und man die Stoffe soweit erhitzen kann, dass die Stoffe schmelzen und sieden können und dann die Moleküle immer noch erhalten bleiben, also auch in der Gasphase als Moleküle vorliegen.
Wenn man sich überlegt, ob ein Molekül unpolar ist kann man auch fragen, warum Moleküle polar sein können. Die Polarität kommt daher, dass die Bindungselektronen einer Atombindung im Molekül von den zwei verbundenen Atome unterschiedlich stark angezogen werden. Daher kann man schon mal folgendes festhalten:
Elektronegativität
An dieser Stelle muss die Elektronegativität angesprochen werden, damit wir diesen Begriff nutzen können und nicht immer so umständlich über unterschiedliche Arten von Atomen sprechen zu müssen.
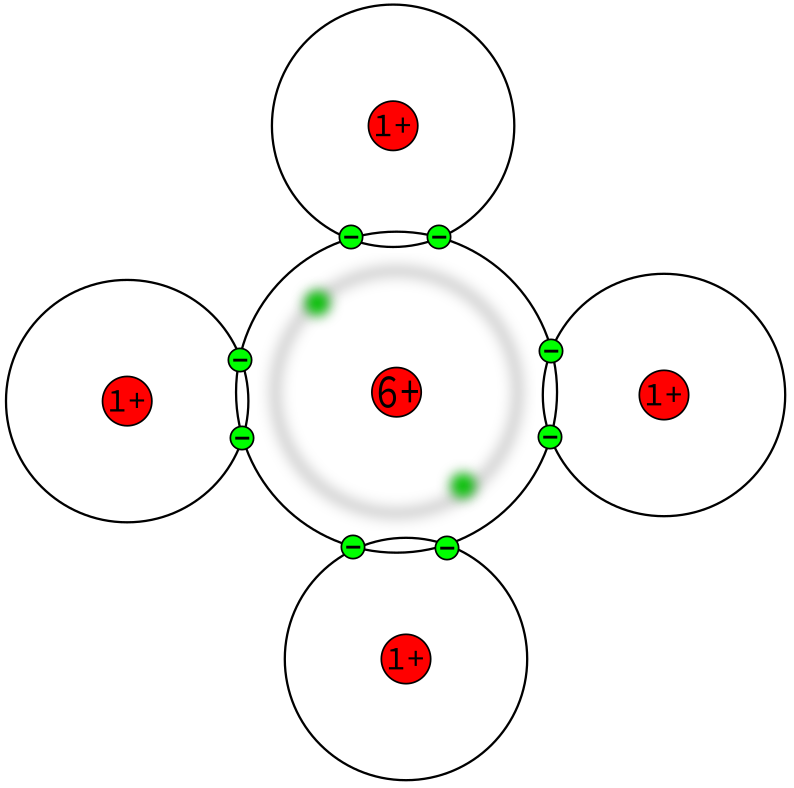
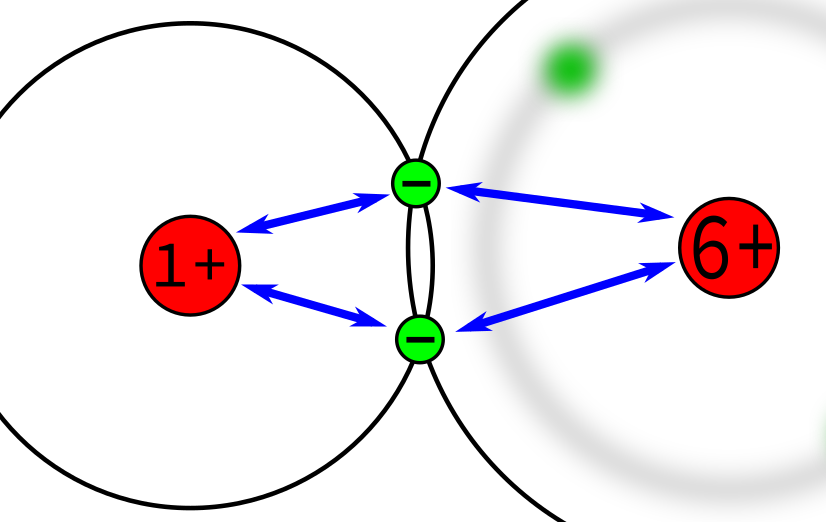
Beim Beispiel Methan CH4, dass zuletzt gezeigt wurde, haben wir unterschiedliche Atome. Im diesem Bild wird gezeigt, wie die Situation bei einer der Bindungen ist.
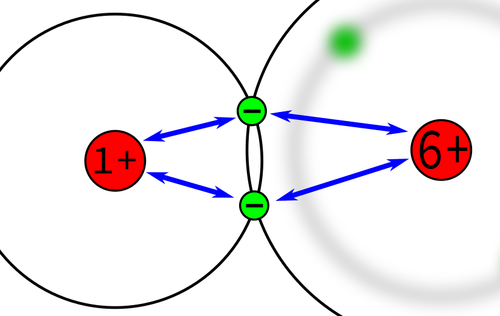
Da das Kohlenstoff-Atom 6 Protonen im Kern hat, im Gegensatz zum Wasserstoff mit nur einem Proton im Kern, zieht der Kern vom Kohlenstoff die Bindungselektronen etwas stärker an. Diese stärkere Anziehung wird als Elektronegativität bezeichnet.
So hat Kohlenstoff, aufgrund der 6 Protonen im Kern, eine höhere Elektronegativität als Wasserstoff:
- EN(C) = 2,5
- EN(H) = 2,3
Die Werte unterscheiden sich jetzt nicht so sehr, wie es angesichts der sehr viel größeren Ladung des Kerns vielleicht zu erwarten wäre. Allerdings hat das damit zu tun, dass beim Kohlenstoff-Atom die Elektronen für die Bindung in der zweiten Schale sind und somit weiter vom kern entfernt sind, als die Bindungselektronen beim Wasserstoff.
Zusammengefasst ist die Elektronegativität von zwei Einflüssen abhängig:
- Je mehr Protonen im Kern ein Atom hat, desto höher ist die Elektronegativität
- Je mehr Schalen die Elektronenhülle hat, desto niedriger ist die Elektronegativität
Das folgende Bild verdeutlichen die EN-Werte im Periodensystem. Aufgrund der Abhängigkeit der Elektronegativität von den zwei Eigenschaften beim Atombau hat Fluor die kleinste Elektronegativität, während Francium die kleinste hat.
In der Periode von Fluor haben die anderen Elemente eine kleinere Elektronegativität, da sie zwar auch recht kleine Atome haben, aber weniger Protonen im Kern. Innerhalb der Hauptgruppe der Halogene hat Fluor die höchste Elektronegativität, weil es zwar nicht so viele Protonen hat, aber dafür kleiner ist.