Wir erforschen den Boden/Messung der Kohlenstoffdioxidabgabe einer Bodenprobe: Unterschied zwischen den Versionen
Main>Cereale Keine Bearbeitungszusammenfassung |
Main>Cereale Keine Bearbeitungszusammenfassung |
||
| Zeile 94: | Zeile 94: | ||
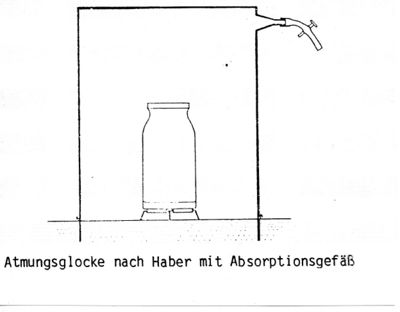
|Bodenbürtiges Kohlenstoffdioxid lässt sich nach Haber mit einer Atmungsglocke direkt an der Erdoberfläche messen . Das Verfahren hat den Nachteil, dass eine differenzierte Messung hinsichtlich der Kohlenstoffdioxidproduktion aus der Wurzel-atmung und der Kohlenstoffdioxidabgabe aus der bakteriellen Atmung nicht möglich ist. Das Verfahren kennzeichnet nur annähernd die natürliche Kohlenstoffdioxidabgabe, weil die Temperatur, die Bodenfeuchtigkeit und die Diffusionsverhältnisse unter der Atmungsglocke gegenüber der freien Bodenoberfläche erheblich verändert werden. | |Bodenbürtiges Kohlenstoffdioxid lässt sich nach Haber mit einer Atmungsglocke direkt an der Erdoberfläche messen . Das Verfahren hat den Nachteil, dass eine differenzierte Messung hinsichtlich der Kohlenstoffdioxidproduktion aus der Wurzel-atmung und der Kohlenstoffdioxidabgabe aus der bakteriellen Atmung nicht möglich ist. Das Verfahren kennzeichnet nur annähernd die natürliche Kohlenstoffdioxidabgabe, weil die Temperatur, die Bodenfeuchtigkeit und die Diffusionsverhältnisse unter der Atmungsglocke gegenüber der freien Bodenoberfläche erheblich verändert werden. | ||
'''Technik des Verfahrens''' | '''Technik des Verfahrens im Freiland''' | ||
Mit einer Atmungslocke wird eine Bodenfläche (z.B. 1 Quadratmeter Bodenfläche) abgedeckt und das Kohlenstoffdioxid in einem Absorptionsgefäß mit Bariumhydroxid aufgefangen. | Mit einer Atmungslocke wird eine Bodenfläche (z.B. 1 Quadratmeter Bodenfläche) abgedeckt und das Kohlenstoffdioxid in einem Absorptionsgefäß mit Bariumhydroxid aufgefangen. | ||
| Zeile 119: | Zeile 119: | ||
Eine einfache Methode des Kohlenstoffdioxidnachweises ist die Bestimmung in einem geschlossenen Gefäß, in dem das Kohlenstoffdioxid in Bariumhydroxidlösung aufgefangen wird. Es bildet sich Bariumcarbonat. Nachfolgend wird die unverbrauchte Lauge gegen Salzsäure (oder Oxalsäure) rücktitriert. | Eine einfache Methode des Kohlenstoffdioxidnachweises ist die Bestimmung in einem geschlossenen Gefäß, in dem das Kohlenstoffdioxid in Bariumhydroxidlösung aufgefangen wird. Es bildet sich Bariumcarbonat. Nachfolgend wird die unverbrauchte Lauge gegen Salzsäure (oder Oxalsäure) rücktitriert. | ||
[[Datei:Weckglas1.jpg|300px| '''Weckglas''']] | [[Datei:Weckglas1.jpg|300px| '''Weckglas''']] | ||
|} | |||
{| class="prettytable" | |||
|<table border="1" width="100%"> | |||
|style="background-color:#EEE9BF ;" | | |||
<h5 align="center">'''Kohlenstoffdioxidmessung im Labor'''</h5> | |||
|- | |- | ||
'''Formeln''' | |||
Ba(OH)2 + CO2 = BaCO3 + H2O | Ba(OH)2 + CO2 = BaCO3 + H2O | ||
Ba(OH)2 + 2 HC1 = BaC12 + 2 H20 | Ba(OH)2 + 2 HC1 = BaC12 + 2 H20 | ||
'''Untersuchungsmaterialien''' | |||
Exsikkator | *Exsikkator | ||
*Waage | |||
schalenförmiges Gefäß (250 ml) für die Bodenprobe | *schalenförmiges Gefäß (250 ml) für die Bodenprobe | ||
schalenförmiges Gefäß (200 ml) für die Bariumhydroxidlösung | *schalenförmiges Gefäß (200 ml) für die Bariumhydroxidlösung | ||
Sieb (2 mm Maschenweite) | *Sieb (2 mm Maschenweite) | ||
Bürette | *Bürette | ||
Pipetten | *Pipetten | ||
REAGENZIEN | '''REAGENZIEN''' | ||
Bariumhydroxid Ba(OH)2 x 8 H20 | Bariumhydroxid Ba(OH)2 x 8 H20 | ||
| Zeile 145: | Zeile 151: | ||
Phenolphthalein (1 prozentig in Ethanol) | Phenolphthalein (1 prozentig in Ethanol) | ||
'''Herstellung der Bariumhydroxidlösung ''' | |||
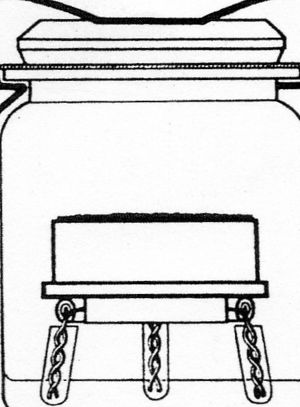
7,17 g Bariumhydroxid und 1 g Bariumchlorid werden in destilliertem Wasser gelöst (auffüllen bis zur 1000 ml Marke). Vom Ungelösten wird abfiltriert. Zur Aufbewahrung der Bariumhydroxidlösung empfiehlt sich eine spezielle Vorrichtung. | 7,17 g Bariumhydroxid und 1 g Bariumchlorid werden in destilliertem Wasser gelöst (auffüllen bis zur 1000 ml Marke). Vom Ungelösten wird abfiltriert. Zur Aufbewahrung der Bariumhydroxidlösung empfiehlt sich eine spezielle Vorrichtung. | ||
Gefäß zur Aufbewahrung von Bariumhydroxidlösung in kohlenstoffdioxidfreier Atmosphäre. Natronkalk ist ein Gemisch aus Ätznatron und Ätzkalk. Er entsteht, wenn man gebrannten Kalk mit Natronlauge löscht. | |||
|} | |||
{| class="prettytable" | |||
|<table border="1" width="100%"> | |||
|style="background-color:#EEE9BF ;" | | |||
<h5 align="center">'''Versuchsablauf'''</h5> | |||
|- | |||
Eine Probe naturfeuchten Bodens wird gesiebt, wobei neben den Grobteilen die Feinwurzeln zum größten Teil entfernt werden. 250 g des gesiebten Bodens werden in eine Schale eingewogen und auf den gelochten Porzellaneinsatz im Exsikkator gestellt. 125 ml Bariumhydroidlösung werden in ein schalenförmiges Gefäß gefüllt und unter die Bodenprobe deponiert. Die Bodenprobe soll möglichst nahe über dem Flüssigkeitsspiegel der Bariumhydroxidlösung stehen. Der Exsikkator wird nun verschlossen. In der Regel sollten mindestens drei Proben und eine Blindprobe ausgewertet werden. Eine Blindprobe , also ein Versuch, bei dem kein Boden eingesetzt wird, ist zwingend erforderlich, um den ursprünglichen Gehalt der Bariumhydroxidlösung an Kohlenstoffdioxid zu bestimmen. | Eine Probe naturfeuchten Bodens wird gesiebt, wobei neben den Grobteilen die Feinwurzeln zum größten Teil entfernt werden. 250 g des gesiebten Bodens werden in eine Schale eingewogen und auf den gelochten Porzellaneinsatz im Exsikkator gestellt. 125 ml Bariumhydroidlösung werden in ein schalenförmiges Gefäß gefüllt und unter die Bodenprobe deponiert. Die Bodenprobe soll möglichst nahe über dem Flüssigkeitsspiegel der Bariumhydroxidlösung stehen. Der Exsikkator wird nun verschlossen. In der Regel sollten mindestens drei Proben und eine Blindprobe ausgewertet werden. Eine Blindprobe , also ein Versuch, bei dem kein Boden eingesetzt wird, ist zwingend erforderlich, um den ursprünglichen Gehalt der Bariumhydroxidlösung an Kohlenstoffdioxid zu bestimmen. | ||
| Zeile 191: | Zeile 181: | ||
Wassergehalt der Bodenprobe ermittelt (siehe Kapitel "Ermittlung der Trockensubstanz einer Bodenprobe"). | Wassergehalt der Bodenprobe ermittelt (siehe Kapitel "Ermittlung der Trockensubstanz einer Bodenprobe"). | ||
Die unverbrauchte Bariumhydroxidlösung wird mit Salzsäure zurücktitriert. Als Indikator werden 3 Tropfen Phenolphthaleinlösung zugesetzt. Der Versuch kann bei Bedarf fortgesetzt werden, indem - jeweils nach Deponierung neuer Bariuntiydroxidlösung - die Kohlenstoffdioxidabgabe über weitere Zeiträume verfolgt wird. | Die unverbrauchte Bariumhydroxidlösung wird mit Salzsäure zurücktitriert. Als Indikator werden 3 Tropfen Phenolphthaleinlösung zugesetzt. Der Versuch kann bei Bedarf fortgesetzt werden, indem - jeweils nach Deponierung neuer Bariuntiydroxidlösung - die Kohlenstoffdioxidabgabe über weitere Zeiträume verfolgt wird. | ||
|} | |||
{| class="prettytable" | |||
|<table border="1" width="100%"> | |||
|style="background-color:#EEE9BF ;" | | |||
<h5 align="center">'''Messung, Auwertung, Auswertungsbeispiel'''</h5> | |||
|- | |||
''' Messung''' | |||
Zur Auswertung wird der Säureverbrauch der Blindprobe vom Säureverbrauch der Bodenprobe subtrahiert. Die Differenz wird mit dem Auswertungsfaktor multipliziert. | Zur Auswertung wird der Säureverbrauch der Blindprobe vom Säureverbrauch der Bodenprobe subtrahiert. Die Differenz wird mit dem Auswertungsfaktor multipliziert. | ||
| Zeile 202: | Zeile 199: | ||
'''Auswertungsbeispiel''' | |||
Kohlenstoffdioxidabgabe von 250 g frischem Boden in 24 | Kohlenstoffdioxidabgabe von 250 g frischem Boden in 24 Stunden: | ||
Stunden: | |||
a) Blindprobe : Es wurden 20 ml 0,02 m Salzsäure verbraucht | a) Blindprobe : Es wurden 20 ml 0,02 m Salzsäure verbraucht | ||
| Zeile 217: | Zeile 212: | ||
12,3 mg Kohlenstoffdioxid-Abgabe je Kilogramm Boden und Tag x 3000 000 kg/ha = 36 900 000 mg CO2 /ha/ Tag = 36,9 kg Kohlenstoffdioxid-Abgabe je Hektar und Tag. | 12,3 mg Kohlenstoffdioxid-Abgabe je Kilogramm Boden und Tag x 3000 000 kg/ha = 36 900 000 mg CO2 /ha/ Tag = 36,9 kg Kohlenstoffdioxid-Abgabe je Hektar und Tag. | ||
'''Die Titration mit Oxalsäure''' | |||
Gewicht der Bodenprobe: 100 g | Gewicht der Bodenprobe: 100 g | ||
| Zeile 229: | Zeile 224: | ||
a) Verbrauch an Oxalsäure für die Blindprobe: 20 ml | a) Verbrauch an Oxalsäure für die Blindprobe: 20 ml | ||
b) Verbrauch an Oxalsäure für die Bodenprobe : 14 | b) Verbrauch an Oxalsäure für die Bodenprobe : 14 ml | ||
(20 ml - 14 ml) x 2,2 = 13,2 mg CO2 / 100g Boden in 24 Stunden | |||
|} | |||
{| class="prettytable" | |||
In der Literatur werden häufig nur 10 g Boden für eine Bodenprobenmenge angegeben. Bei einfacher Laborausstattung ist es zweckmäßig, die Bodenmenge auf 200 oder 250 g zu erhöhen. Bei mehrtägiger Versuchsdauer sollte die Bariumhydroxidlösung gelegentlich leicht geschüttelt werden, um die Bildung einer absorptionshemmenden Carbonathaut auf der Lösung zu verhindern. Anstelle von Salzsäure und Oxalsäure können auch andere eingestellte Säuren für die Titration verwendet werden. | |<table border="1" width="100%"> | ||
|style="background-color:#EEE9BF ;" | | |||
<h5 align="center">'''Erfahrungen und Konsequenzen'''</h5> | |||
|- | |||
|In der Literatur werden häufig nur 10 g Boden für eine Bodenprobenmenge angegeben. Bei einfacher Laborausstattung ist es zweckmäßig, die Bodenmenge auf 200 oder 250 g zu erhöhen. Bei mehrtägiger Versuchsdauer sollte die Bariumhydroxidlösung gelegentlich leicht geschüttelt werden, um die Bildung einer absorptionshemmenden Carbonathaut auf der Lösung zu verhindern. Anstelle von Salzsäure und Oxalsäure können auch andere eingestellte Säuren für die Titration verwendet werden. | |||
{{Kasten_rot|}} | |||
<H4>Sicherheitshinweis</h4> | |||
Oxalsäure ist giftig! Die Verwendung von Pipettierhilfen ist zu kontrollieren! | Oxalsäure ist giftig! Die Verwendung von Pipettierhilfen ist zu kontrollieren! | ||
{{Kasten_rot||}} | |||
Version vom 16. März 2009, 13:13 Uhr
Messung der Kohlenstoffdioxidabgabe einer Bodenprobe
|