Chemie/Sammlung von Experimenten/Energiebetrachtung bei Kupfersulfat
Wir haben bei diesem Experiment die Möglichkeit, eine Reaktion und ihre Umkehrreaktion recht einfach zu beobachten und den Energieumsatz zu erkennen.
Sicherheitsinformationen
Wie üblich gilt bei der Verwendung des Bunsenbrenners entsprechende Schutzmaßnahmen zu ergreifen.
Die verwendete Chemikalie Kupfersulfat ist wassergefährdend, d.h. sie darf nicht ins Abwasser gelangen. Die Chemikalien können außerdem wiederverwendet werden und sollen daher nicht weggeworfen werden. Der Hautkontakt mit dem Kupfersulfat sollte vermieden werden, die Schutzbrille schützt auch vor einem Augenkontakt! Für den Fall eines Kontaktes soll die Haut mit viel Wasser abgewaschen werden.
Materialien
- Stativ mit Muffe, Stativklammer mit befestigtem Thermometer (Messbereich 0° bis 100°)
- Zwei saubere und trockene Abdampfschalen.
- Wasserfreies Kupfersulfat
- Wasserhaltiges Kupfersulfat
- Bunsenbrenner mit Dreibein und Keramiknetzauflage
- Tiegelzangen zum Anfassen der heißen Abdampfschale nach dem Erhitzen.
- Papiertücher zum Abwischen der Abdampfschalen zum Schluss.
- Smartphone, um Fotos zu machen.
Durchführung
1. Teilexperiment: Reaktion von wasserfreiem Kupfersulfat mit Wasser
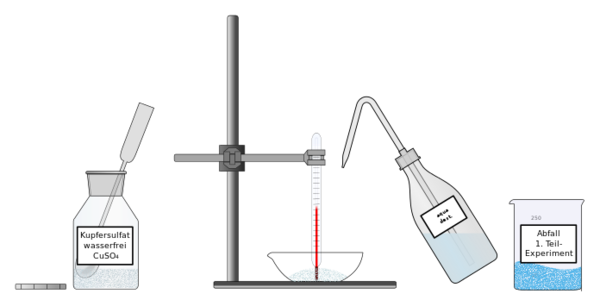
Entnimm aus dem Vorratsgefäß etwas weißes Kupfersulfat und gib es in eine saubere und trockene Abdampfschale. Die Menge sollte aussreichen, dass bei dem Thermometer das Ausdehnungsgefäß unten komplett im Kupfersulfat steckt. Dazu kann man durchaus das Kupfersulfat auch anhäufen.
Verschiebe das Thermometer nun am Stativ nach unten bis das Ausdehnungsgefäß im Kupfersulfat "steckt". Gib nun in kleinen Mengen Wasser aus der Spritzflasche auf das Kupfersulfat und beobachte das Kupfersulfat und die Temperatur.
- ACHTUNG: Das Kupfersulfat soll nur leicht angefeuchtet und nicht aufgelöst werden!
Gib weiter vorsichtig Wasser dazu, bis sich die Temperatur nicht mehr verändert.
2. Teilexperiment:
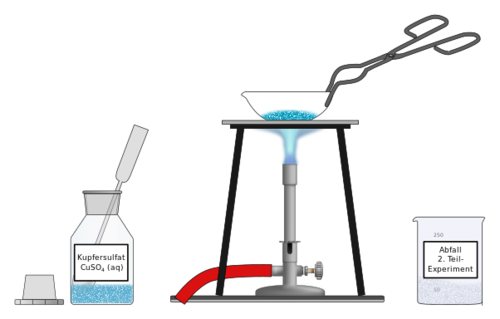
Entnimm etwa die gleiche Menge an blauem Kupfersulfat, wie du sie vorher im ersten Teilexperiment verwendet hast, und gebe es in eine saubere und trockene Abdampfschale. Stelle die Abdampfschale auf das Drahtnetz über den Bunsenbrenner und erhitze das Kupfersulfat mit rauschender Flamme. Beobachte die Veränderungen, höre auch hin. Wenn sich das Kupfersulfat nicht mehr verändert, kannst du aufhören, es zu erhitzen.
Warte kurz, bis sich die Abdampfschale etwas abgekühlt hat und fasse die Abdampfschale nur mit der Tiegelzange an.
Entsorgung und Reinigung der Gefäße
Die Abdampfschalen sollen nicht mit Wasser ausgewaschen werden bevor das Kupfersulfat daraus entfernt wurde.
Es reicht den Abfall in die jeweiligen Bechergläser zu schütten bzw. leicht mit einem Spatel abzukratzen. Den "Reinigungs"-Spatel nach der Nutzung mit etwas Papier abwischen, ebenso die benutzten Gefäße.
Bitte alles wieder ordentlich sortieren und wegstellen, so dass die nächsten Schüler wissen, was sie brauchen.
Auswertung nach der Durchführung des Experiments
Gefährdungsbeurteilung
Zu diesem Experiment existiert eine Gefährdungsbeurteilung. Download







